题目内容
【题目】如图所示,A~H 分别是氢、氧、氮、氯、碳、钠、镁 、钙八种元素中的两种或几种组成的初中化学常见物质。“→”箭头表示物质间能转化,“﹣”表示物质间能反应),C、E是常用的灭火剂。请回答:

(1)G、E的化学式为___、____。
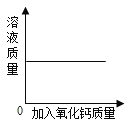
(2)C和_____(填物质名称) 反应可生成D。
(3)写出下列化学方程式:A→B:_____。F和H反应:_____。
【答案】Na2CO3 CO2 氧化钙 HCl+AgNO3=AgCl↓+HNO3 2NaOH+ Mg(NO3)2=Mg(OH)2↓+2NaNO3或2NaOH+MgCl2=Mg(OH)2↓+2NaCl
【解析】
A~H 分别是氢、氧、氮、氯、碳、钠、镁、钙八种元素中的两种或几种组成的初中化学常见物质,A、B是酸,根据题中提供的元素组成的酸是盐酸和硝酸,A以转化为B,盐酸与硝酸银反应生成氯化银和硝酸,所以A是盐酸,B是硝酸;C、E是常用的灭火剂、氧化物,E能转化为C,二氧化碳、水是常用的灭火剂、氧化物,二氧化碳与氢氧化钙反应生成碳酸钙和水,所以E是二氧化碳,C是水; C能转化为D(碱),根据题中提供的元素,水与氧化钙反应生成氢氧化钙,所以D是氢氧化钙;D(氢氧化钙)能转化为F(碱),根据题中提供的元素,碳酸钠与氢氧化钙反应生成氢氧化钠和碳酸钙,所以F是氢氧化钠;F(氢氧化钠)能与H(盐)反应,根据题中提供的元素,氢氧化钠能与硝酸镁(或氯化镁)反应生成氢氧化镁和硝酸钠(或氯化钠),所以H是硝酸镁或氯化镁;E(二氧化碳)能转化为G(盐),根据题中提供的元素,二氧化碳与氢氧化钠反应生成碳酸钠和水,所以G是碳酸钠。经过验证,推导正确。
根据以上分析可知:
(1)G是碳酸钠、E是二氧化碳,化学式分别为Na2CO3、CO2;
(2)C和氧化钙 反应可生成D;
(3)A→B的反应是盐酸和硝酸银反应生成氯化银沉淀和硝酸,化学方程式为::HCl+AgNO3=AgCl↓+HNO3;
F和H的反应是氢氧化钠和硝酸镁反应生成氢氧化镁沉淀和硝酸钠,或氢氧化钠和氯化镁反应生成氢氧化镁沉淀和氯化钠,化学方程式分别为:2NaOH+ Mg(NO3)2=Mg(OH)2↓+2NaNO3或2NaOH+MgCl2=Mg(OH)2↓+2NaCl。

 教学练新同步练习系列答案
教学练新同步练习系列答案 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
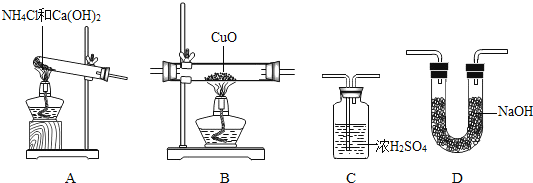
倍速训练法直通中考考点系列答案【题目】如图所示,烧瓶内盛有x气体,若挤压滴管的胶头a,使液体y进入烧瓶中,振荡烧瓶,并倒放在铁架台上,将导管伸入滴有z的水中,打开弹簧夹b,可见烧杯中的液体如喷泉一样喷入烧瓶中,并出现颜色的改变.则x、y、z可能是( )
选项 | |||
A | O2 | H2SO4 | 紫色石蕊试液 |
B | CO2 | H2O | 无色酚酞试液 |
C | CO | Ca(OH)2 | 紫色石蕊试液 |
D | CO2 | NaOH | 无色酚酞试液 |

A.A B.B C.C D.D
【题目】小明为研究金属X、Zn、Fe、Cu的活动性顺序,做了如下实验:
(1)将金属X分别放入ZnSO4、FeSO4、CuSO4的溶液中,反应后有无金属析出的情况如下表所示:
溶液种类 | ZnSO4 | FeSO4 | CuSO4 |
加入X后有无金属析出 | 无 | 无 | 有 |
则金属X、Cu和Fe的活动性顺序由强到弱排列为_____。
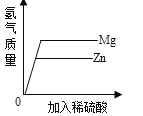
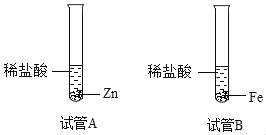
(2)小明继续研究Zn和Fe的活动性强弱,将质量相等的颗粒大小相同的金属Zn和Fe放在少量的相同体积的同种稀盐酸中,如图所示,若出现_____的现象,则Zn的活动性比Fe强;
(3)小军通过将Fe放入CuSO4溶液反应,也可比较出Cu和Fe的活动性强弱,请写出Fe和CuSO4的化学方程式_____。