题目内容
【题目】甲、乙两位同学在学习甲烷的性质时,发现甲烷与氢气和一氧化碳在性质上有很多相似之处,如密度比空气小,难溶于水,具有可燃性等。但H2和CO都具有还原性,那么甲烷有没有还原性呢?为了验证甲烷是否具有还原性,乙同学设计以下实验装置并进行实验探究:
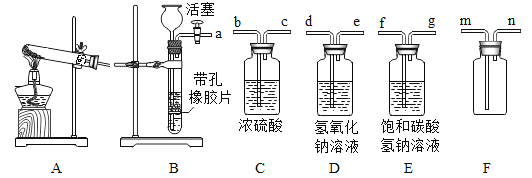
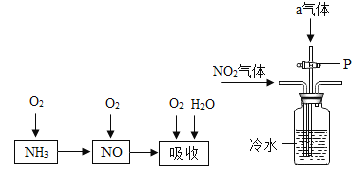
[实验装置]
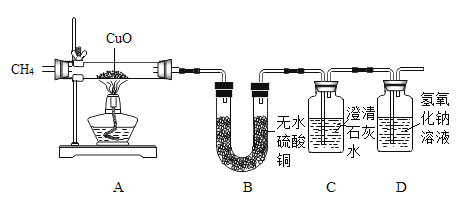
[查阅资料]白色无水CuSO4遇水变蓝,有吸水性。
[实验步骤](假设药品都是足量的,氢氧化钠溶液的作用是防止空气中的CO2进入装置C)
①分别称量装置A、B、C的质量;②向玻璃管中装入CuO;③先通一段时间的CH4,再加热装置A,使其充分反应;④停止加热,继续通入CH4至玻璃管冷却到室温;⑤再次分别称量装置A、B、C的质量。
先通一段时间的CH4,再加热装置A的目的是_____。甲同学认为还缺少一个步骤,缺少的步骤是_____。
[进行实验]乙同学按照正确的步骤进行实验,并记录了实验现象和数据
装置A中的黑色粉末变红;装置B中白色粉末变蓝;装置C中石灰水变浑浊;称量数据如下表所示
装置A中玻璃管(含药品)的质量 | 装置B的质量 | 装置C的质量 | |
反应前 | 150g | 156.6g | 256.8g |
反应后 | 147.2g | 158.4g | 257.9g |
[现象分析与数据处理]
根据装置ABC中的现象可推知,CH4与CuO充分反应后的产物依次是_____、_____、_____。
[实验结论]
(1)CH4_____ (填“有”或“没有”)还原性。
(2)根据实验数据,甲同学提出甲烷与氧化铜反应的产物中还有一氧化碳,生成一氧化碳的质量为_____克。
(3)装置A中发生反应的化学方程式为_____。
【答案】排尽空气,以免加热时发生爆炸 检查装置的气密性 Cu H2O CO2 有 0.7 ![]()
【解析】
[实验步骤] 先通一段时间的CH4,再加热装置A的目的是排尽空气,防止甲烷和空气的混合气体受热而发生爆炸。为防止装置漏气影响实验结果,甲同学认为还缺少一个步骤,缺少的步骤是检查装置的气密性;
[进行实验]装置A中的黑色粉末变红,说明氧化铜被还原生成了铜,固体减少的质量即为参加反应的氧化铜中氧元素的质量=150g-147.2g=2.8g;装置B中白色粉末变蓝,说明有水生成,B装置增加的量即为生成水的质量=158.4g-156.6g=1.8g;装置C中石灰水变浑浊说明生成二氧化碳,增加的量为生成二氧化碳的质量=257.9g-256.8g=1.1g;
[现象分析与数据处理]
根据装置ABC中的现象可推知,CH4与CuO充分反应后的产物依次是铜、水、二氧化碳;
[实验结论]
(1)由反应现象可知,CH4夺取了氧,具有还原性;
(2)根据质量守恒定律可知,反应前后元素的种类、质量不变。生成二氧化碳中碳元素的质量为1.1g![]() =0.3g,则氧元素=0.8g;生成的水中氢元素的质量为=1.8g
=0.3g,则氧元素=0.8g;生成的水中氢元素的质量为=1.8g![]() =0.2g,则氧元素=1.6g;则C:H=3:2, 而甲烷中C:H=4:1,因此可知,还生成了一氧化碳,生成一氧化碳的质量为(2.8g-0.8g-1.6g)÷
=0.2g,则氧元素=1.6g;则C:H=3:2, 而甲烷中C:H=4:1,因此可知,还生成了一氧化碳,生成一氧化碳的质量为(2.8g-0.8g-1.6g)÷![]() =0.7g,且其中碳元素的质量为0.3g;
=0.7g,且其中碳元素的质量为0.3g;
(3)根据质量守恒定律反应前后元素的种类、质量不变可知,参加反应的甲烷的质量为:0.3g+0.3g+0.2g=0.8g,氧化铜的质量为:2.8g÷![]() 14g,则生成铜的质量为14g-2.8g=11.2g,即甲烷、氧化铜、铜、水、一氧化碳、二氧化碳的质量比为:0.8g:14g:11.2g:1.8g:0.7g:1.1g,装置A中发生反应的化学方程式为
14g,则生成铜的质量为14g-2.8g=11.2g,即甲烷、氧化铜、铜、水、一氧化碳、二氧化碳的质量比为:0.8g:14g:11.2g:1.8g:0.7g:1.1g,装置A中发生反应的化学方程式为![]() 。
。