��Ŀ����
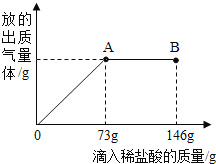
����Ŀ����֪Na2CO3��ˮ��Һ�ʼ�������һ�ձ���ʢ��20.4g Na2CO3�� NaCl ��ɵĹ����������������μ������ʷ���Ϊ 10%��ϡ�������ų�������� ������������ϡ�����������ϵ������ͼ��ʾ�����������ش����⣺
(1)���μ�ϡ������ͼ�� B ��ʱ���ձ�����Һ�� pH______7(������=����)��
(2)���μ�ϡ������ͼ�� A ��ʱ���ձ���Ϊ��������Һ(����)��ͨ��������� �������ʵ���������___________��(����������һλС��)
���𰸡� �� 24.2%
��������(1)��ͼ��֪�����μ�ϡ������A��ʱ��������ȫ��Ӧ�����Ե��μӵ�B��ʱ������������ձ�����Һ��PH��7��(2)��μ�ϡ���ᵽAʱ���ų����������ΪX���μӷ�Ӧ��̼���Ƶ�����ΪY�����ɵ��Ȼ��Ƶ�����ΪZ���������֪�����μӵ�Aʱ�������Ȼ����������73g��10%�T7.3g����
Na2CO3+2HCl�T2NaCl+H2O+CO2��
106 73 117 44
Y 7.3g Z X
![]() �� Y�T10.6g
�� Y�T10.6g
![]() ��Z�T11.7g
��Z�T11.7g
![]() ��X�T4.4g
��X�T4.4g
����Ϊ�Ȼ��ƣ��Ȼ��Ƶ�����Ϊ��11.7g+20.4g-10.6g�T21.5g��
��Һ������Ϊ��20.4g+73g-4.4g�T89g��
�������ʵ���������Ϊ�� ![]() ��100%�T24.2%��
��100%�T24.2%��

����Ŀ��ijУ�о���ѧϰС���ͬѧ�����һ���Ա�ʵ�飬̽����������ˮʱ�Ƿų�����������������������ͼA��B��C����ʵ��װ����ʢ��һ����ˮ��С�Թ������μ������NaCl��NH4NO3��NaOH(�����������֮ǰ������ʵ��װ����U�ι����˵�Һ���ƽ)��
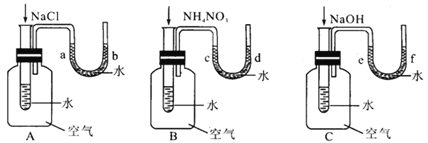
(1)���������������
A | B | C | |
���� | ___________ | ____________ | ___________ |
ԭ�� | __________ | ____________ | ____________ |
(2)�����������ܽ���ˮ�ĶԱ�ʵ������ó��ij���������______________��