题目内容
【题目】金属材料与我们生活息息相关
(1)从物质分类角度看,合金属于_____(填“纯净物”或“混合物”)
(2)将硬铝片和铝片相互刻画,____(填“硬铝”或“铝”)片上留下明显划痕。
(3)“辽宁”号航母舰体外壳涂上防锈漆可防止生锈,其原理是_______。
(4)锂电池广泛用于手机和笔记本电脑等电子产品中。锂﹣氯化银电池反应的 化学方程式为 Li+AgCl═LiCl+Ag,可知 Li 的金属活动性比 Ag 的______(填“强”或 “弱”)
(5)钢是铁的合金。取 11.4g 钢样,向其中加入足量稀硫酸,产生氢气 0.4g(不 考虑钢样中其他成分与稀硫酸的反应)。此钢样中铁的质量分数_____百分 数保留一位小数)
【答案】 混合物 铝 隔绝水和氧气 强 98.2%
【解析】(1)合金属于混合物;(2)合金的硬度大于纯金属,故铝的表面有划痕;(3)舰体外壳涂上防锈漆可防止生锈是因为能隔绝水和氧气; (4)锂能把银置换出来,说明锂的活动性强于银; (5)设钢样中铁的质量为x
Fe+H2SO4=FeSO4+H2↑
56 2
x 0.4g
![]()
x=11.2g
此钢样中铁的质量分数为:11.2g11.4g×100%≈98.2%。

【题目】四位同学元旦去礐石风景区游玩,带回了几小块石灰石样品。为了检测样品中碳酸钙的含量,甲、乙、丙、丁四位同学用浓度相同的盐酸与样品充分反应来进行实验测定,(样品中的杂质不溶于水,且不与盐酸反应)测定数据如下:
甲同学 | 乙同学 | 丙同学 | 丁同学 | |
所取石灰石样品质量(g) | 10.0 | 10.0 | 10.0 | 10.0 |
加入盐酸的质量(g)烧杯中 | 10.0 | 20.0 | 30.0 | 40.0 |
剩余物质的总质量(g) | 19.0 | 28.0 | 37.0 | 46.7 |
试回答:
(1)四位同学里面,______同学的实验样品完全反应;10.0g石灰石样品与 _______g盐酸恰好完全反应。
(2)求样品中碳酸钙的质量分数为___________(写出计算过程)。
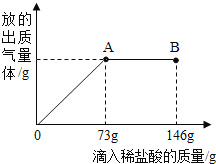
(3)请在图中画出加入稀盐酸的质量与生成气体的质量的变化关系(标注必要的数值)。
 ___________
___________