题目内容
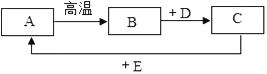
【题目】已知A、B、C、D、E是初中化学中常见的不同类别的物质,它们之间的关系如图所示(“→”表示物质间的转化关系,“—”表示两端的物质能发生化学反应)。A是使用最广泛的金属,C是常用的食品干燥剂,E是配制波尔多液的主要成分之一,其溶液为蓝色,F是由三种元素组成的化合物,请回答下列问题:

(1)写出下列物质的化学式:B____________,E____________,F____________
(2)物质C所属的物质类别是____________,选择C作为食品干燥剂的原因有____________(答一条即可)。
(3)写出D转化为F的化学方程式:____________________________________。
(4)B在生产上的用途有________________________,上述反应没有包含的基本反应类型是_______________________。
【答案】H2SO4 CuSO4 NaOH 氧化物 价格低廉 Ca(OH)2+Na2CO3=CaCO3↓+2NaOH 金属除锈 分解反应
【解析】
A是使用最广泛的金属,即为Fe,C为常用的食品干燥剂,可假设为CaO,E是配制波尔多液的主要成分之一,其溶液为蓝色,即为CuSO4,B可与金属Fe、金属氧化物CaO反应,并且物质的类别与上述几种物质不同,推断为酸,又因为B可转化为CuSO4,则B为H2SO4,D物质的类别与上述几种物质不同,推断为碱,由CaO可转化为D可知,D为Ca(OH)2。F可由Ca(OH)2转化得到,可假设F是含Ca2+盐或者碱等,又因F可与CuSO4反应,F应为碱,Ca(OH)2与Na2CO3反应产物之一为NaOH,因此F为NaOH。
(1)通过上述分析可知,B为H2SO4,E为CuSO4,F为NaOH。
(2)物质C为CaO,属于氧化物,CaO可与水反应吸收包装中的水分,CaO价格低廉都是其作为食品干燥剂的原因。
(3)D物质为Ca(OH)2,F物质为NaOH,由上述分析Ca(OH)2可与Na2CO3反应生成NaOH和CaCO3沉淀,化学方程式为Ca(OH)2+Na2CO3=2NaOH+CaCO3↓
(4)B物质为H2SO4,可用于金属除锈;上述反应中Fe与H2SO4的反应为置换反应,H2SO4与Ca(OH)2的反应为复分解反应,CaO可与水制取Ca(OH)2,该反应为化合反应,故上述反应中没有的基本反应类型是分解反应。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】下表是Ca (OH)2和NaOH的溶解度数据,下列说法正确的是
温度/°C | 0 | 20 | 40 | 60 | 80 | 100 | |
溶解度/g | Ca (OH)2 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 |
NaOH | 31 | 91 | 111 | 129 | 313 | 336 | |
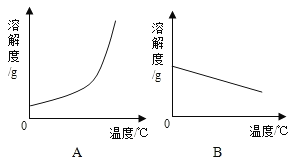
A.图中能表示NaOH溶解度曲线的是B
B.蒸发水可将饱和的Ca (OH)2溶液变为不饱和溶液
C.20 °C时向Ca (OH)2的饱和溶液中加入少量生石灰,恢复到20 °C后,溶液中溶质的质量分数不变
D.80°C时,饱和的Ca (OH)2和NaOH溶液中,前者所含溶质质量少于后者