题目内容
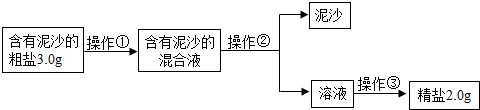
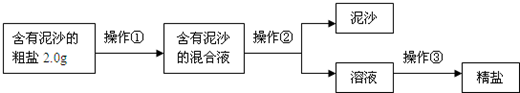
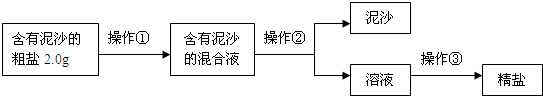
某化学兴趣小组设计出下列粗盐提纯的实验方案,请你一起来完成以下问题.
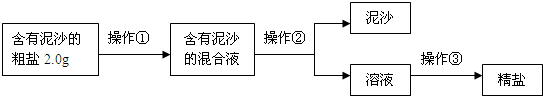
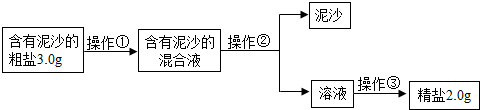
(1)操作①②③的名称依次是______、______、______,在实施操作①前需先将粗盐磨碎,其作用是______,同时该操作①所需水的最佳量是______(已知20℃时食盐的溶解度是36g,填字母序号).
A 5mL B 8mL C 12mL
(2)操作②所需的玻璃仪器有______,若该操作结束后发现溶液仍浑浊,则可能原因是______(任答一点原因,即可);
(3)实施操作③时玻璃棒要不断______(填操作方法),直到______时停止加热.
(4)兴趣小组的同学通过正确的计算发现,实验所得精盐的产率比该粗盐中氯化钠的实际含量偏低,则可能的原因是______(填字母序号)
A.过滤时滤纸有破损 B.蒸发时有固体溅出
C.溶解含有泥沙的粗盐时,加入的水量不足
D.将含有泥沙的混合液全部倾倒入过滤器后,用清水洗涤玻璃棒和烧杯并将该液体一并倒入过滤器
E.转移精盐时,玻璃棒、蒸发皿中有残留的固体
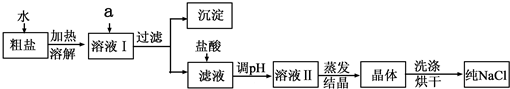
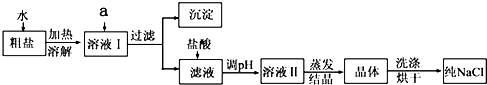
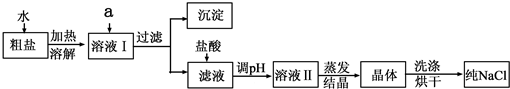
(5)兴趣小组成员查阅资料后得知,粗盐中除含NaCl、泥沙外,还含有少量MgCl2、CaCl2、Na2SO4等杂质.而过滤是一种将______与水分离的方法,因此上一套实验方案不能除去粗盐中的MgCl2、CaCl2、Na2SO4等杂质,为此,他们又重新设计了第二套实验方案.
提供的试剂有:Na2CO3溶液、K2CO3溶液、NaOH溶液、BaCl2溶液、Ba(NO3)2溶液、饱和NaCl溶液.
①欲除去溶液I中的MgCl2、CaCl2、Na2SO4,从提供的试剂中选出a所代表的试剂,按滴加顺序依次为:过量的NaOH溶液、过量的______、过量的______;
②在滤液中加盐酸的作用是______;
(6)该兴趣小组现利用提纯后的精盐配制200g溶质质量分数为0.9%的生理盐水,需要精盐的质量为______g,配制该溶液时所需要的水应选择______(选填“50mL”、“100mL”或“500mL”)量筒,读数时,若视线仰视(其他操作无误),则所配制的溶液的溶质质量分数______(选填“大于”、“小于”或“等于”)0.9%.
解:(1)先通过沉降把大的颗粒除去,再通过过滤将不溶于液体的固体与液体分离,蒸发是将水分除去得到精盐;将粗盐磨碎,其作用是便于溶解并除去其中的杂质;假设2g全部是食盐再根据食盐的溶解度可计算出需要水5.56mL,所以所需水的最佳量为8mL,
(2)过滤用到的仪器有:漏斗、烧杯、玻璃棒、铁架台,所以所需的玻璃仪器有漏斗、烧杯、玻璃棒;溶液仍浑浊,则可能原因是滤纸破损、烧杯很脏、滤液高于滤纸边缘;
(3)蒸发使用玻璃棒搅拌,防止局部温度过高使液滴飞溅,待大部分固体析出,停止加热,靠余热将剩余固体结晶析出;
(4)所得精盐的产率比该粗盐中氯化钠的实际含量偏低说明食盐少了,符合这一点都可以,过滤时滤纸有破损导致粗盐中杂质也进入食盐,导致食盐质量增加,产率会偏高,蒸发时有固体溅出会导致食盐减少,溶解含有泥沙的粗盐时,加入的水量不足会导致一些杂质进入食盐,质量分数会偏大,将含有泥沙的混合液全部倾倒入过滤器后,用清水洗涤玻璃棒和烧杯并将该液体一并倒入过滤器,这是正确操作,没有误差,转移精盐时,玻璃棒、蒸发皿中有残留的固体,导致食盐量减少;
(5)过滤是除去不溶于液体的固体的;①除去杂质MgCl2、CaCl2、Na2SO4实际是除去镁离子、钙离子、硫酸根离子,将它们沉淀出来即可,除去镁离子用氢氧根离子、除去钙离子用碳酸根离子、除去硫酸根离子用钡离子,又因为不能引入新的杂质,所以加入氢氧化钠、碳酸钠、氯化钡即可,又因为碳酸钠是除去氯化钙和过量的氯化钡的,所以碳酸钠必须放到氯化钡的后面;②据盐酸可以与碳酸钠和氢氧化钠反应,所以盐酸是除去过量的氢氧化钠和碳酸钠的;③精盐质量:200g×0.9%=1.8g;需水200g-1.8g=198.2g所以选择大于该数还最接近的,用500mL量筒;读数时,若视线仰视量取的水偏多,所以溶质质量分数偏小.
故答案为:(1)沉降;过滤;蒸发;便于溶解并除去其中的杂质;B;(2)烧杯、漏斗、玻璃棒;滤纸破损;(3)搅拌;大部分固体结晶析出;(4)BCE;(5)泥沙;①BaCl2溶液;碳酸钠溶液;②除去过量的碳酸钠和氢氧化钠;(6)1.8;500mL;小于.
分析:(1)根据混合物分离的方法,假设2g全部是食盐再根据食盐的溶解度考虑需要水的量;(2)根据过滤用到的仪器和仍很浑浊的原因考虑;(3)根据蒸发时的注意事项考虑;(4)所得精盐的产率比该粗盐中氯化钠的实际含量偏低说明食盐少了,符合这一点都可以;(5)根据过滤的特点考虑;①根据除去MgCl2、CaCl2、Na2SO4杂质,产生沉淀,且不能引进其他杂质考虑;②根据盐酸可以与碳酸钠和氢氧化钠反应考虑;(6)根据溶质的计算方法和量筒的选取方法考虑,根据仰视读数量取水的体积大小考虑误差.
点评:通过回答本题知道了混合物分离的方法和除去可溶性杂质的方法,不能引入新的杂质,并且注意顺序.
(2)过滤用到的仪器有:漏斗、烧杯、玻璃棒、铁架台,所以所需的玻璃仪器有漏斗、烧杯、玻璃棒;溶液仍浑浊,则可能原因是滤纸破损、烧杯很脏、滤液高于滤纸边缘;
(3)蒸发使用玻璃棒搅拌,防止局部温度过高使液滴飞溅,待大部分固体析出,停止加热,靠余热将剩余固体结晶析出;
(4)所得精盐的产率比该粗盐中氯化钠的实际含量偏低说明食盐少了,符合这一点都可以,过滤时滤纸有破损导致粗盐中杂质也进入食盐,导致食盐质量增加,产率会偏高,蒸发时有固体溅出会导致食盐减少,溶解含有泥沙的粗盐时,加入的水量不足会导致一些杂质进入食盐,质量分数会偏大,将含有泥沙的混合液全部倾倒入过滤器后,用清水洗涤玻璃棒和烧杯并将该液体一并倒入过滤器,这是正确操作,没有误差,转移精盐时,玻璃棒、蒸发皿中有残留的固体,导致食盐量减少;
(5)过滤是除去不溶于液体的固体的;①除去杂质MgCl2、CaCl2、Na2SO4实际是除去镁离子、钙离子、硫酸根离子,将它们沉淀出来即可,除去镁离子用氢氧根离子、除去钙离子用碳酸根离子、除去硫酸根离子用钡离子,又因为不能引入新的杂质,所以加入氢氧化钠、碳酸钠、氯化钡即可,又因为碳酸钠是除去氯化钙和过量的氯化钡的,所以碳酸钠必须放到氯化钡的后面;②据盐酸可以与碳酸钠和氢氧化钠反应,所以盐酸是除去过量的氢氧化钠和碳酸钠的;③精盐质量:200g×0.9%=1.8g;需水200g-1.8g=198.2g所以选择大于该数还最接近的,用500mL量筒;读数时,若视线仰视量取的水偏多,所以溶质质量分数偏小.
故答案为:(1)沉降;过滤;蒸发;便于溶解并除去其中的杂质;B;(2)烧杯、漏斗、玻璃棒;滤纸破损;(3)搅拌;大部分固体结晶析出;(4)BCE;(5)泥沙;①BaCl2溶液;碳酸钠溶液;②除去过量的碳酸钠和氢氧化钠;(6)1.8;500mL;小于.
分析:(1)根据混合物分离的方法,假设2g全部是食盐再根据食盐的溶解度考虑需要水的量;(2)根据过滤用到的仪器和仍很浑浊的原因考虑;(3)根据蒸发时的注意事项考虑;(4)所得精盐的产率比该粗盐中氯化钠的实际含量偏低说明食盐少了,符合这一点都可以;(5)根据过滤的特点考虑;①根据除去MgCl2、CaCl2、Na2SO4杂质,产生沉淀,且不能引进其他杂质考虑;②根据盐酸可以与碳酸钠和氢氧化钠反应考虑;(6)根据溶质的计算方法和量筒的选取方法考虑,根据仰视读数量取水的体积大小考虑误差.
点评:通过回答本题知道了混合物分离的方法和除去可溶性杂质的方法,不能引入新的杂质,并且注意顺序.

练习册系列答案
相关题目