题目内容
【题目】汽车安全气囊中常含有NaHCO3、Fe2O3、NaN3、KClO4等物质,当发生碰撞时,它们立即反应产生大量气体,使气囊迅速膨胀而起到保护作用。
(1)NaHCO3俗称_____,由Na+和_____(填离子符号)构成;KClO4中Cl元素的化合价为_____。
(2)在药剂遭受撞击时,NaN3首先分解为金属 Na 和一种常见的气体单质,该气体的化学式为_____。
(3)KClO4溶液是一种常用的化学分析试剂。现欲配制100g质量分数为10%的KClO4溶液,过程如下图所示:
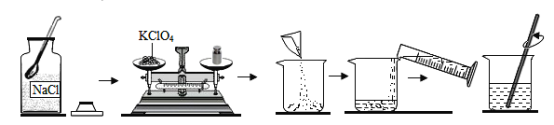
实验过程中需称量_____gKClO4固体,使用的仪器主要有_____、托盘天平、烧杯、玻璃棒、药匙等。
(4)NaHCO3受热时生成CO2、H2O和纯碱。请写出该反应的化学方程式_____。
【答案】小苏打 HCO3- +7 N2 10.0 量筒 ![]()
【解析】
(1)NaHCO3是碳酸氢钠的化学式,碳酸氢钠俗称为小苏打,由Na+ 和HCO3-构成;KClO4中K的化合价为+1,O的化合价为-2,根据化合物中化合价的代数和为0,设氯元素化合价为x,(+1)+x+(-2) ×4=0,得出Cl的化合价为+7。
(2)在遭受撞击时,NaN3分解为金属Na和一种常见的气体单质,根据元素组成可以得出这种气体单质为氮气,化学式为N2。
(3)配制100g质量分数为10%的KClO4溶液,需要称量KClO4固体的质量=![]() ,使用的仪器主要有量筒、托盘天平、烧杯、玻璃棒、药匙等。
,使用的仪器主要有量筒、托盘天平、烧杯、玻璃棒、药匙等。
(4)纯碱是碳酸钠的俗称,NaHCO3受热时生成CO2、H2O和碳酸钠,化学方程式为![]() 。
。

 阅读快车系列答案
阅读快车系列答案【题目】某同学发现上个月做实验用的氢氧化钠溶液忘记了盖瓶盖。对于该溶液是否变质,该同学对此进行了探究。请你一起完成下列实验报告。
(1)(提出问题1)该溶液是否变质?
(实验探究1)
实验步骤 | 实验现象 | 解释与结论 |
取少量该溶液放于试管中,滴加足量稀盐酸 | 有____产生 | 说明该溶液已变质,变质的原因是_____(请用化学方程式表示) |
(2)(提出问题2)该溶液变质程度怎样?
(提出猜想)猜想一:已完全变质,该溶液中溶质只含Na2CO3 猜想二:部分变质,该溶液中溶质含有_____
(查阅资料)氯化钡溶液呈中性。
(实验探究2)
实验步骤 | 实验现象 | 结论 |
先取少量该溶液放于试管中,加入过量氯化钡溶液 | 有____生成 | 猜想____成立 |
静置,取上层清液于另一支试管中,加入2-3滴酚酞溶液 | 上层清液变红 |
(3)反思:在(实验探究2)中加入过量的氯化钡溶液的目的是什么?___________________。
(4)拓展:除去部分变质的氢氧化钠溶液中的杂质,方法是___________________(用化学方程式表示)。
(5)提升:为进一步探究氢氧化钠的变质程度,小明称取 18.6 g 氢氧化钠固体样品放入烧杯中,向其中逐滴加入稀盐酸,到不再产生气泡为止,共消耗稀盐酸 100 g,反应后称得烧杯中溶液的质量为 114.2 g。该氢氧化钠的变质程度(即变质的氢氧化钠占变质前的氢氧化钠的质量分数为)__________________。