��Ŀ����
����Ŀ��ij��ѧ������ȤС����̽��̼���ƺ�̼�����Ƶ�ʱ����������ͼװ�õ�ʵ�顣
ʵ����Ʒ����ͬ�ͺŵ�U��2֧����Ƥ��2����10mLһ����ע����2֧������2����
ʵ���������U���зֱ����0.53g̼���ƺ�̼�����ƹ��壬����֧ע�����зֱ�������ͬ����������������ͬ���������ϡ���ᡣ��ע������Ƥ���У�Ȼ��ͬʱѸ�ٽ�����ֱ�ע��U���С�
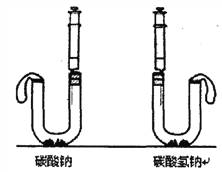
̼����+ϡ���� | ̼������+ϡ���� | |
ʵ������ | Ѹ�ٲ����϶����ݣ��������� | ________________ |
ʵ����� | ̼������̼�����ƾ�����ϡ���ᷴӦ�������� | |
���ݷ�����ͨ������˵����������̼���ƺ�̼�����ƣ��������ʲ���������̼�����ࣿ(Ҫ�м������)________________________
���𰸡� Ѹ�ٲ����������ݣ������������ʿ� ��������̼���ƺ�̼��������������ϡ���ᷴӦ���ɵĶ�����̼��̼�����ƶ�
��������������Ҫ�����˸��ݻ�ѧ����ʽ�ļ��㡣
��1��̼�����Ʊ�̼���Ƶķ�Ӧ�ٶȿ죬���Ѹ�ٲ������������������������ʿ죻
��2���裺0.53g̼�����ܹ����ɶ�����̼������Ϊx��
Na2CO3+2HCl=2NaCl+H2O+CO2��
106 44
0.53g x
![]() ��� x=0.22g
��� x=0.22g
�裺0.53g̼�������ܹ����ɶ�����̼������Ϊy��
NaHCO3+HCl=NaCl+H2O+CO2��
84 44
0.53g x
![]() y=0.28g��y>x
y=0.28g��y>x
��������������̼���ƺ�̼��������������ϡ���ᷴӦ���ɵĶ�����̼��̼�����ƶࡣ