题目内容
【题目】实验室中有一包由KCl、MgSO4和CaCl2组成的固体混合物,某校研究性学习小组的同学为了除去其中的MgSO4和CaCl2,得到纯净的KCl,设计了如下实验方案。
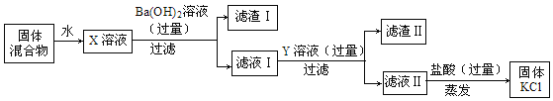
请你回答下列问题:
(1)X溶液与Ba(OH)2溶液反应的化学方程式是 ,该反应所属的基本反应类型是 。
(2)Y溶液中溶质的化学式是 。
(3)该实验中盐酸的作用是 。
【答案】(1)Ba(OH)2+MgSO4===BaSO4↓+Mg(OH)2↓,复分解反应。
(2)K2CO3。
(3)除去滤液Ⅱ中的KOH和多余的K2CO3
【解析】(1)由KCl、MgSO4和CaCl2三种物质中国硫酸镁能与氢氧化钡反应生成硫酸钡沉淀和氢氧化镁沉淀,Ba(OH)2 + MgSO4 ===BaSO4 ↓+Mg(OH)2 ↓,由两种化合物相互交换成分形成两种新的化合物的反应叫复分解反应。(2)除去氯化钙得到更多的氯化钾K2CO3 ,应用碳酸钾溶液,碳酸钾和氯化钙反应生成碳酸钙沉淀和氯化钾。(3)滤液Ⅱ中有过量的氢氧化钾和碳酸钾,二者都能与盐酸反应生成氯化钾,所以加入过量的盐酸的目的是除去滤液Ⅱ中的KOH和多余的K2CO3

练习册系列答案
相关题目