题目内容
【题目】用化学方程式回答下列问题。
(1)碳酸氢铵夏天存放质量减少 __________________________________。
(2)用氨水处理含稀硫酸的废水____________________________________。
(3)用氢氧化钠溶液吸收二氧化硫__________________________________。
(4)实验室用锌和硫酸反应制氢气__________________________________。
(5)城市居民使用天然气作为燃料__________________________________。
(6)潜水艇使用过氧化钠(Na2O2)与二氧化碳反应生成碳酸钠与氧气作为氧气再生原理_____。
【答案】 NH4HCO3![]() NH3↑+H2O+CO2↑ 2NH3H2O+H2SO4=(NH4)2SO4+2H2O 2NaOH + SO2 ==Na2SO3 + H2O Zn + H2SO4 == ZnSO4 + H2↑ CH4 + 2O2
NH3↑+H2O+CO2↑ 2NH3H2O+H2SO4=(NH4)2SO4+2H2O 2NaOH + SO2 ==Na2SO3 + H2O Zn + H2SO4 == ZnSO4 + H2↑ CH4 + 2O2 ![]() CO2 + 2H2O 2Na2O2 +2CO2= 2Na2CO3+O2↑
CO2 + 2H2O 2Na2O2 +2CO2= 2Na2CO3+O2↑
【解析】本题考查了书写化学方程式的能力,化学方程式书写时需要注意的是正确书写化学式、配平、条件的标注、符号标注等。
(1)碳酸氢铵夏天存放质量减少是由于碳酸氢铵分解生成了氨气、水和二氧化碳,化学方程式是:NH4HCO3![]() NH3↑+H2O+CO2↑;
NH3↑+H2O+CO2↑;
(2)氨水与稀硫酸反应生成硫酸铵和水,化学方程式是:2NH3H2O+H2SO4=(NH4)2SO4+2H2O;
(3)氢氧化钠与二氧化硫反应生成亚硫酸钠和水,化学方程式是:2NaOH + SO2 ==Na2SO3 + H2O;
(4)锌和硫酸反应生成硫酸锌和氢气,化学方程式是:Zn + H2SO4 == ZnSO4 + H2↑;
(5)天然气的主要成分是甲烷,甲烷在氧气中燃烧生成水和二氧化碳,CH4 + 2O2 ![]() CO2 + 2H2O;
CO2 + 2H2O;
(6)过氧化钠(Na2O2)与二氧化碳反应生成碳酸钠与氧气,化学方程式是:2Na2O2 +2CO2= 2Na2CO3+O2↑。

【题目】某化学课外兴趣小组在探究碳酸钠和碳酸氢钠的时候,做过如下图装置的实验。
实验用品:相同型号的U型管2支、橡皮塞2个、10mL一次性注射器2支、气球2个。
实验操作:在U型管中分别加入0.53g碳酸钠和碳酸氢钠固体,在两支注射器中分别吸入相同溶质质量分数、相同体积的足量稀盐酸。将注射器橡皮塞中,然后同时迅速将盐酸分别注入U型管中。
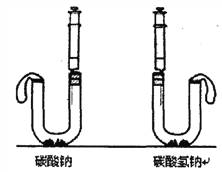
碳酸钠+稀盐酸 | 碳酸氢钠+稀盐酸 | |
实验现象: | 迅速产生较多气泡,气球膨胀 | ________________ |
实验结论 | 碳酸钠与碳酸氢钠均能与稀盐酸反应产生气体 | |
数据分析:通过计算说明等质量的碳酸钠和碳酸氢钠,哪种物质产生二氧化碳质量多?(要有计算过程)________________________