题目内容
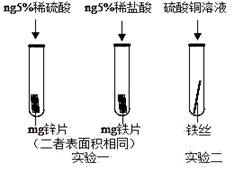
现有银、铜、铁三种金属,某研究小组为探究银、铜、铁的金属活动性顺序,设计了三
个实验:(Ⅰ)将铁片浸入稀硫酸中;(Ⅱ)将银片浸入稀硫酸中;(Ⅲ)将铁片浸入硫酸铜溶液中。
实验(Ⅲ)中反应的化学方程式为 ;该反应的基本类型为 反应
上述三个实验还不能完全证明三种金属的活动性顺序,请你补充一个实验来达到实验目的(写出实验操作和现象) 。根据以上探究,三种金属的活动性由强到弱的顺序是 。
Fe + CuSO4 =" Cu" + FeSO4 置换 将银片浸入硫酸铜溶液中,无明显现象 Fe Cu Ag。
解析试题分析:铁比铜活泼,所以铁能将铜置换出来,反应类型为置换反应,由以上三个实验可知,Fe大于Cu,Fe大于银,但无法确定Cu和Ag,所以可将Ag 浸入硫酸铜中观察到无明显现象,说明Ag 小于Cu,从而得到三种金属的活动性由强到弱的顺序是Fe Cu Ag
考点:金属活动顺序的应用及其测定。

练习册系列答案
 作业辅导系列答案
作业辅导系列答案 同步学典一课多练系列答案
同步学典一课多练系列答案 经典密卷系列答案
经典密卷系列答案 金牌课堂练系列答案
金牌课堂练系列答案
相关题目
下列有关铜、铁、铝的说法正确的是( )
| A.缺铁性贫血里所说的铁是指铁元素 |
| B.黄铜不是合金,而是纯金属 |
| C.铝是地壳中含量最高的元素 |
| D.人类最早大规模使用的金属是 |
人类的生产生活离不开金属。
(1)在地壳里含量最多的金属元素是 。
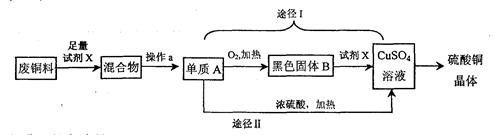
(2)我国是世界上最早使用湿法炼铜的国家,其反应原理是 。(用
化学方程式表示)。下列铜制品的用途中,利用金属导电性的是 (填字母)。
| A.铜火锅 | B.铜导线 | C.铜钟 | D.铜钱 |
露在空气中也容易被锈蚀的,铜锈的化学式为Cu2(OH)2CO3,其
生锈的条件与铁有相似之处,另外,还可能与空气中的 有关。
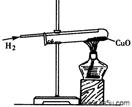
(4)下图是实验室用氢气还原氧化铜实验的示意图。实验结束后,某同学发现试管里红色的物质又变成黑色,原因是 。

 CO2↑+CO↑+H2O。某化学兴趣小组同学设计如下实验装置,用于制取纯净干燥的CO气体来还原氧化铁。请根据题目要求回答下列问题:
CO2↑+CO↑+H2O。某化学兴趣小组同学设计如下实验装置,用于制取纯净干燥的CO气体来还原氧化铁。请根据题目要求回答下列问题:
