题目内容
【题目】某化学兴趣小组为了测定鸡蛋壳中碳酸钙的含量,进行了如下实验:取25.0g洗净、粉碎后的鸡蛋壳样品放于烧杯中,向烧杯中滴加稀盐酸(整个过程不考虑盐酸的挥发和气体的溶解),实验测得烧杯中剩余物质的质量与加入盐酸的质量之间的关系如图所示
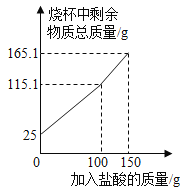
求:(1)产生CO2的总质量为____________g。
(2)鸡蛋壳中碳酸钙的质量分数________________。
【答案】 9.9 90%.
【解析】解:(1)根据质量守恒定律可知反应前后减少的质量就是生成二氧化碳的质量,产生CO2的总质量为25g+150g-165.1g=9.9g;(2)设鸡蛋壳中碳酸钙的质量是x,则:
CaCO3+2HCl═CaCl2+CO2↑+H2O
100 44
x 9.9g
![]()
x=22.5g,
鸡蛋壳中碳酸钙的质量分数=![]() ×100%=90%,
×100%=90%,
答:(1)产生CO2的总质量为9.9g;(2)鸡蛋壳中碳酸钙的质量分数为90%。

练习册系列答案
 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案
相关题目
【题目】(1)写出下列符号中“2”的意义:
①Mg2+__________;
②![]() _________;
_________;
③O2__________。
(2)按要求用数字和化学符号填空。
1个水分子 | 2个氢原子 | 3个氧离子 | 4个钾原子 |
_______ | _______ | ________ | ________ |