题目内容
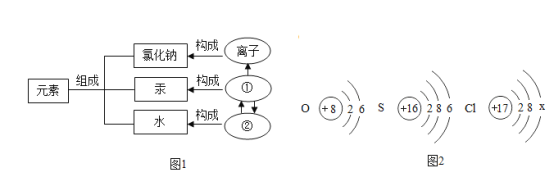
【题目】为了探究物质的化学性质,某兴趣小组做了如图1所示实验。实验结束后,小组同学将A、B两支试管中的上层清液倒进一洁净的烧杯中,观察到一会儿后才有气泡产生,然后有白色沉淀生成(如图2)。
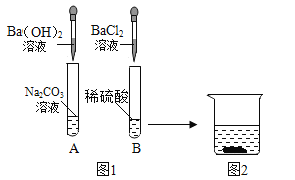
请回答下列问题:
(1)Na2CO3溶液呈_____性;
(2)B试管中出现的现象是_____;
(3)A试管中的物质充分反应后,所得溶液的溶质有_____;
(4)写出烧杯中有气泡产生的反应的化学方程式_____。
【答案】碱 生成白色沉淀 Na2CO3、NaOH ![]()
【解析】
(1)Na2CO3俗称纯碱,溶液呈碱性;
(2)B试管中氯化钡与稀硫酸反应产生硫酸钡和盐酸,硫酸钡是不溶于盐酸的白色固体,则实验现象是:生成白色沉淀;
(3)A试管中氢氧化钡与碳酸钠反应产生氢氧化钠和碳酸钡沉淀,B试管氯化钡与稀硫酸反应产生硫酸钡沉淀和稀盐酸,将A、B两支试管中的上层清液倒进一洁净的烧杯中,观察到一会儿后才有气泡产生,因为A试管中的氢氧化钠与B试管中的稀盐酸反应,无明显现实,一会后,稀盐酸将氢氧化钠反应完全,与碳酸钠反应,产生二氧化碳气体;最后B试管中过量的氯化钡溶液与A试管中的碳酸啊反应产生碳酸钡白色沉淀生成,则A试管中的物质充分反应后,所得溶液的溶质有:Na2CO3、NaOH;
(4)烧杯中碳酸钠与稀盐酸反应产生氯化钠、水和二氧化碳的化学方程式:![]() 。
。

 智能训练练测考系列答案
智能训练练测考系列答案【题目】化学实验室常用到氢氧化钠溶液,当多次揭开其瓶盖后,同学们猜想该试剂可能变质了,在征得老师同意后,开展了以下探究:
[提出问题1]该瓶氢氧化钠溶液是否变质了?
[实验探究1]
实验操作 | 实验现象 | 实验结论 |
取少量该溶液于试管中,滴加足量稀盐酸 | _____, | 氢氧化钠溶液一定变质了 |
该步骤中发生反应的化学方程式为_____。
[提出问题2]该瓶氢氧化钠溶液是全部变质还是部分变质呢?
[查阅资料]氯化钙溶液、氯化钠溶液均星中性,碳酸钠溶液星碱性。
[实验探究2]
实验操作 | 实验现象 | 实验结论 |
①取少量该溶液于试管中,滴加过量的CaCl2溶液,并不断振荡 | _____, | 原溶液中一定含有Na2CO3 |
②取步骤①试管中的少量上层清液.滴加酚酞溶液 | 溶液变为红色 | 原溶液中一定含有_____, |
[反思评价] .
(1)上述步骤①中滴加过量CaCl2溶液的目的是_____。
(2)在上述[实验探究2]中,小明提出可用氢氧化钙溶液代替氯化钙溶液,你认为该方案_____,(填“可行”或“不可行”),原因是_____。