题目内容
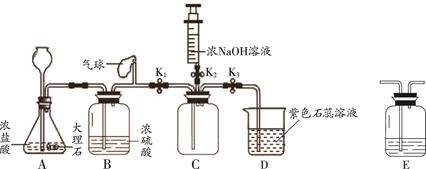
使用浓硫酸时要十分小心,浓硫酸有强烈的 !所以,不要将浓硫酸沾到皮肤或衣服上。为了加深记忆,小丽同学用下图形象地总结了硫酸能与5类物质发生反应。请你根据要求完成下列问题。
(1)将紫色石蕊溶液滴入稀硫酸溶液中,紫色石蕊溶液遇稀硫酸变成 ;
(2)稀硫酸能够除铁锈(铁锈的主要成分Fe2O3),除锈后溶液颜色的变化情况是 ,
写出反应的化学方程式 ;
(3)为了验证反应⑤能够发生,应选择的物质是 ;
| A.NaCl溶液 | B.NaOH溶液 |
| C.Ba(NO3 )2溶液 | D.MgCl2溶液 |
腐蚀性 (1) 红色
(2) 溶液由无色变成黄色 Fe2O3 + 3H2SO4 === Fe2(SO4)3 + 3H2O
(3) C (4) Fe + H2SO4 = FeSO4 + H2↑ Fe + CuSO4 === FeSO4 + Cu
解析试题分析:稀硫酸呈酸性,能使紫色石蕊溶液变红;酸能与金属氧化物反应,稀硫酸与氧化铁反应生成硫酸铁和水,溶液有无色变成黄色;验证反应是否能够进行,最好选择有明显现象的物质间的反应,如硫酸与硝酸钡反应会生成白色沉淀,硫酸虽然能与NaOH溶液反应,但没有明显现象,可借助指示剂来判断反应的发生;铁与稀硫酸反应生成硫酸亚铁和氢气,要除去硫酸亚铁溶液中含少量硫酸铜,可铁与硫酸铜发生置换反应除去。
考点:硫酸的性质

 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案(5分)某实验小组利用废硫酸液制备K2SO4的流程如下:
⑴ 将CaCO3研成粉末的目的是 。
⑵ 上述流程中可循环使用的物质有CO2和 (填写化学式)。
⑶ 反应Ⅲ中相关物质的溶解度如下表所示。你认为反应Ⅲ在常温下能实现的原因是
。
| 物质 | KCl | K2SO4 | NH4Cl | M |
| 溶解度/g(25℃) | 34.0 | 11.1 | 37.2 | 19.5 |
a.AgNO3溶液 b.过量的BaCl2溶液 c.过量的Ba(NO3)2溶液
(4分)亚硝酸钠是一种食品添加剂,按照《食品添加剂使用卫生标准》规定,食品中允许添加限量为70mg/kg,不可超量、超范围使用。亚硝酸钠外观酷似食盐且有咸味,如果将亚硝酸钠(NaNO2)误作食盐食用或摄入过量亚硝酸盐后,可引起中毒,甚至死亡。亚硝酸钠和食盐的有关资料如下:
| 项目 | 亚硝酸钠(NaNO2) | 氯化钠(NaCl) |
| 水溶性 | 易溶,在15℃时溶解度为81.5g | 易溶,在15℃时溶解度为35.8g |
| 熔 点 | 271℃ | 801℃ |
| 沸 点 | 320℃会分解,放出有刺鼻气味的气体 | 1413℃ |
| 跟稀盐酸作用 | 放出红棕色的气体NO2 | 无反应 |
① ;
② 。
(2)亚硝酸钠有咸味,外形与食盐很相似,其水溶液显碱性,食盐的水溶液呈中性。根据以上叙述,鉴别亚硝酸钠溶液和食盐溶液应选用的试剂是 。
(3)亚硝酸钠跟盐酸反应会生成氯化钠、两种氮的氧化物(NO2、NO)和水,请你写出亚硝酸钠跟盐酸反应的化学方程式为 。