题目内容
【题目】小芳对复分解反应发生的条件产生兴趣,于是她和小组内同学仅用以下药品展开了探究。
实验药品:稀硫酸、稀盐酸、氢氧化钠溶液、碳酸钠溶液、硝酸钡溶液、氯化钠溶液、酚酞试液
(提出问题)复分解反应发生的条件是什么?
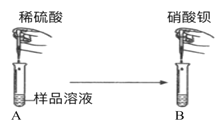
(查阅资料)硝酸钡溶液显中性,且Ba2+有毒。
(实验探究)小芳用上述物质做了下列几组实验
组合序号 | (1) | (2) | (3) | (4) | (5) | (6) |
组合物质 | 稀盐酸 氯化钠 | 稀盐酸 氢氧化钠 | 稀盐酸 碳酸钠 | 稀硫酸 硝酸钡 | 氯化钠 硝酸钡 | 硝酸钡 碳酸钠 |
(记录和解释)
(1)组合(1)、(2)、(5)均无明显现象,其中组合___________与另外两组的实质不同。为证明该不同之处,小芳在实验过程中使用了酚酞试液。
(2)请写出组合(6)的化学方程式___________。
(实验结论)他们通过实验探究并请教老师后知道,只有当两种化合物互相交换成分,生成物中有___________生成时,复分解反应才可以发生。
(拓展延伸)实验结束后,他们将所有废液收集在废液缸中静置,观察到白色沉淀和无色的上层清液。为了确定沉淀和清液的成分,继续展开探究。
(实验1)探究沉淀的成分。
(提出猜想)I.沉淀只有硫酸钡 II.___________, III.沉淀中含有硫酸钡和碳酸钡
小莲取少量沉淀于试管中,滴加过量的___________(请补充完整实验操作和观察到的现象),证明了猜想III是正确的。
(实验2)探究清液的成分。
①取少量清液于试管中,向其中滴加硝酸钡溶液,无明显现象。
②另取少量清液于另一只试管中,滴加___________,有白色沉淀产生。
(解释与结论)探究活动结束后,小组内成员通过讨论分析,一致认为清液中一定没有的离子是___________(指示剂除外,且不考虑水的电离)。
(处理废液)为了防止污染环境,小芳对废液进行处理,将固体回收进一步处理,溶液排放。
(交流与反思)根据你对复分解反应发生条件的了解,请写出一个题中实验药品间除(1)~(6)组合之外,能发生复分解反应的化学方程式___________。
【答案】(2) ![]() 沉淀或气体或水 沉淀只有碳酸钡 稀盐酸,沉淀部分溶解,有气泡产生 稀硫酸(或Na2CO3溶液); OH-、CO32-、 SO42-、H+
沉淀或气体或水 沉淀只有碳酸钡 稀盐酸,沉淀部分溶解,有气泡产生 稀硫酸(或Na2CO3溶液); OH-、CO32-、 SO42-、H+ ![]()
【解析】
记录和解释:(1)稀盐酸和氯化钠不反应,因此无明显现象,稀盐酸和氢氧化钠反应生成氯化钠和水,无明显现象,氯化钠和硝酸钡不反应,无明显现象,故(1)、(5)是因为没有反应。而无明显现象,(2)发生了反应,故与另外两组的实质不同的是(2)
(2)硝酸钡与碳酸钠反应生成碳酸钡和硝酸钠,该反应的化学方程式为:![]() ;
;
实验结论:复分解反应的条件是:只有当两种化合物互相交换成分,生成物中有沉淀、气体、水生成时,复分解反应才可以发生;
实验1:
提出猜想:将所有废液收集在废液缸中静置,出现白色沉淀,这些物质中,只有硝酸钡能与碳酸钠反应生成碳酸钡沉淀,硝酸钡和硫酸反应生成硫酸钡沉淀,故白色沉淀可能是碳酸钡,也可能是硫酸钡,也可能是碳酸钡和硫酸钡的混合物,故Ⅱ、沉淀只有碳酸钡;
结论为猜想III是正确的,故沉淀为碳酸钡和硫酸钡的混合物,碳酸钡能与稀盐酸反应生成氯化钡、二氧化碳和水,硫酸钡与稀盐酸不反应,故可滴加过量稀盐酸,沉淀部分溶解,有气泡产生,说明含碳酸钡和硫酸钡;
实验2:
②有沉淀产生,由以上分析可知,废液中只能产生硫酸钡、碳酸钡沉淀,有沉淀产生,说明清液中含钡离子,故可加入稀硫酸或碳酸钠;
解释与结论:①取少量清液于试管中,向其中滴加硝酸钡溶液,无明显现象。钡离子能与硫酸根离子结合成硫酸钡沉淀,也能与碳酸根离子结合生成碳酸钡沉淀,故无明显现象,说明溶液中不含硫酸根离子和碳酸根离子;
由②可知,含有钡离子;
将所有废液收集在废液缸中静置,观察到白色沉淀和无色的上层清液,无色上层清液,说明不含氢氧根离子,因为无色酚酞遇碱变红,由以上分析可知,白色沉淀中含碳酸钡,故上层清液中不含氢离子,因为氢离子能与碳酸钡反应,不能共存。
故清液中一定没有的离子是:OH-、CO32-、 SO42-、H+;
交流反思:由所给试剂可以看出,稀硫酸也能与氢氧化钠反应生成硫酸钠和水,该反应符合“两种化合物互相交换成分生成另外两种化合物”的反应,属于复分解反应,该反应的化学方程式为:![]() 。
。

 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案【题目】在一个密闭的容器内有四种物质,在一定条件下充分反应,测得反应前后各物质的质量,数据见下表.下列说法错误的是( )
物 质 | 甲 | 乙 | 丙 | 丁 |
反应前质量/g | 2 | 20 | 14 | 2 |
反应后质量/g | m | 28 | 0 | 8 |
A.m的值是2B.甲可能是该反应的催化剂
C.反应的乙、丁质量比是4:3D.该反应是化合反应