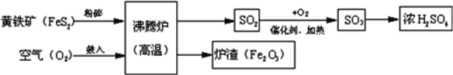题目内容
【题目】我国科学家建立国家尺度的氮足迹混合分析方法,来评价生命周期的氮流动。如图是氮元素在元素周期表的信息,下列判断不正确的是( )
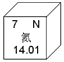
A.氮元素属于非金属元素
B.氮原子核外有2个电子层
C.氮的相对原子质量为14.01
D.化学反应中,氮原子易失去电子
【答案】D
【解析】
在原子中,质子数=核外电子数,最外层电子数大于4,在反应中易得到电子,最外层电子数小于4,在反应中易失去电子。
A、氮元素是气字旁,属于非金属元素,故A正确;
B、氮原子是质子数为7,核外有2个电子层,故B正确;
C、汉字下面的数字表示相对原子质量,氮的相对原子质量为14.01,故C正确;
D、氮原子最外层电子数为5,化学反应中,氮原子易得到电子,故D不正确。故选D。

 中考解读考点精练系列答案
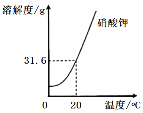
中考解读考点精练系列答案【题目】(1)请根据下列实验和溶解度曲线回答问题(已知水的密度约为1 g/cm3)
实验操作 | 实验结果 |
|
取100 mL水,加入25 g硝酸钾,搅拌恢复至20℃ | 全部溶解,得溶液A | |
再加w g硝酸钾,搅拌,恢复到20℃ | 恰好饱和,得溶液B | |
再加25 g硝酸钾,搅拌,恢复到20℃ | 得溶液C | |
加热 | 全部溶解,得溶液D | |
冷却至20℃ | 析出晶体,得溶液E |
①表中w的值为__________。
②一定属于不饱和溶液的是______(填序号)。
③溶质的质量分数一定相等的溶液是B和___(填序号),此时溶质的质量分数是___(精确到0.01%)。
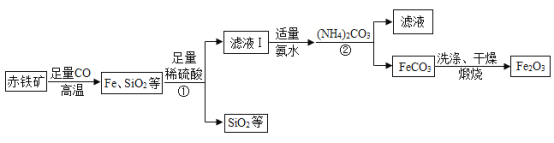
(2)许多果农用钼素去促进东魁杨梅优质丰产;金属元素钼(Mo)通常用作合金及不锈钢的添加剂。化工生产中制备金属钼的主要流程如下图:
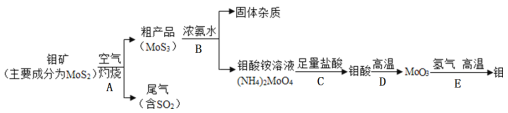
①步骤A中,灼烧钼矿通常会将矿石粉碎成小颗粒,其目的是__________________。
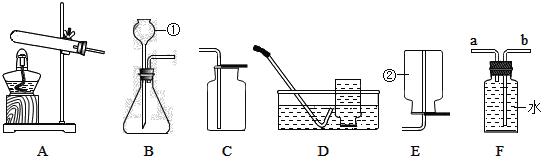
②现有:a烧杯b玻璃棒c漏斗d酒精灯等四种仪器,如果在实验室模拟步骤B,则不需要选用的是_____(填字母序号)。
③写出步骤E的化学方程式______________________________。