��Ŀ����
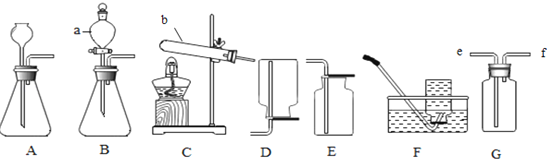
����Ŀ��A��F��Ŀǰ������ѧ�ļ��ֳ��������ʣ���������ͼ��ʾ��ת����ϵ�����ֻ�ѧ��Ӧ�ķ�Ӧ��������Ӧ�������δ����������֪B�Ǻ�ɫ��ĩ��D�ܹ���ֲ�������������F�ǿ�������Ⱦ������֮һ��������Ԫ�ص�������Ϊ1��1������Ӧ����������ͨ�硣
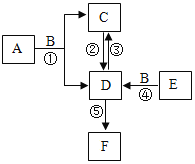
��ش��й����⣺
��1��д���й��������ƣ�A_____��D_____ E_____
��2��д����Ӧ�������ı�ʾʽ�����û�ѧʽ��ʾ��
��Ӧ����_____
��Ӧ����_____
��Ӧ����_____
��Ӧ����_____
��Ӧ����_____
��3����Ӧ���Ļ�ѧ��Ӧ����������_____
��4��B�����ڷ�Ӧ�٢�����_____���á�
���𰸡�����������Һ ���� ����� 2H2O2![]() 2H2O+O2�� 2H2O
2H2O+O2�� 2H2O![]() 2H2��+O2�� 2H2+O2
2H2��+O2�� 2H2+O2![]() 2H2O 2KClO3
2H2O 2KClO3![]() 2KCl+3O2�� S+O2
2KCl+3O2�� S+O2![]() SO2 �ֽⷴӦ ��
SO2 �ֽⷴӦ ��
��������
��1��A��F��Ŀǰ������ѧ�ļ��ֳ��������ʣ�B�Ǻ�ɫ��ĩ��D�ܹ���ֲ�����������D��������������F�ǿ�������Ⱦ������֮һ��������Ԫ�ص�������Ϊ1��1��������E�Ƕ�������Ӧ����������ͨ�磬Cͨ�����������������C��ˮ��A��B��Ӧ������ˮ������������A�ǹ���������Һ��B�Ƕ������̣�E�Ͷ������̷�ӦҲ����������������E������أ�������֤���Ƶ���ȷ������A�ǹ���������Һ��D������ E������أ��������������Һ ���� ����أ�
��2����Ӧ���ǹ��������ڶ������̵Ĵ�����������ˮ����������ѧ����ʽΪ��2H2O2![]() 2H2O+O2�������2H2O2
2H2O+O2�������2H2O2![]() 2H2O+O2����
2H2O+O2����
��Ӧ����ˮ��ͨ��������·ֽ�������������������ѧ����ʽΪ��2H2O![]() 2H2��+O2�������2H2O
2H2��+O2�������2H2O![]() 2H2��+O2����
2H2��+O2����
��Ӧ���������������ڵ�ȼ������������ˮ��2H2+O2![]() 2H2O�����2H2+O2
2H2O�����2H2+O2![]() 2H2O��
2H2O��
��Ӧ����������ڶ������̵Ĵ������¼��������Ȼ��غ���������ѧ����ʽΪ��2KClO3![]() 2KCl+3O2�������2KClO3
2KCl+3O2�������2KClO3![]() 2KCl+3O2����
2KCl+3O2����
��Ӧ������������ڵ�ȼ�����������ɶ�������ѧ����ʽΪ��S+O2![]() SO2�����S+O2
SO2�����S+O2![]() SO2��
SO2��
��3����Ӧ����������ڶ������̵Ĵ������¼��������Ȼ��غ����������Ի�ѧ��Ӧ���������ǷֽⷴӦ������ֽⷴӦ��
��4��B�����ڷ�Ӧ�٢���������ã��������

 ��Կ���Ծ�ϵ�д�
��Կ���Ծ�ϵ�д�����Ŀ����ѧ��ȤС��̽������������ʱ����һ��ȥ������Ĥ��þ��������һ������ϡ�����У������ݲ�������ַ�Ӧ���ã������Թ����лҰ�ɫ������д���������ݵķ�Ӧ��ѧ����ʽ______��
��������⣩�Ұ�ɫ������ʲô���ʣ�
��������裩��С����Ϊ�Ұ�ɫ����Ϊ̼��þ��MgCO3��������ͬѧ��Ϊ����Ҫʵ����ܷ�С���IJ��룬������_____________________��
��С����Ϊ���ڷ�Ӧ���Ȼ�þ��������ƫ�࣬�Ұ�ɫ����Ϊ�������ܽ���Ȼ�þ���塣
��Сͮ��Ϊ�Ұ�ɫ����Ϊ__________________��
��ʵ��̽��1��
ʵ����� | ���� | ���� |
��ȡ�Թ��е��ϲ���Һ�������������Ȼ�þ���� | �Ȼ�þ����__��ѡ�����ܽ����������ܽ����� | С�������� |
��ȡ������ɫ������������ϡ������ | û������ð�� | Сͮ������� |
��������̽���������ԭ�в������˷�
���������ϣ�
HCl+AgNO3�THNO3+AgCl����AgCl��һ�ְ�ɫ�������Ȼ������������壬��ʹ��ɫʯ����ֽ��졣����
��ʵ��̽��2��
��������ȡ�Ұ�ɫ���������Թ��м��ȣ���պ����������Һ�IJ����������Թ��ڣ��������ϵ���Һ���ְ�ɫ���ǣ�֤��������__���塣��μ�����������_______��ʵ�鲽�衢�����ۣ���
ͬѧ�������ʦ���֪��������þ��ϡ���ᷴӦʱ����Һ�ᾭ�������Ե������Ҽ�������ǿ�Ĺ��̣��Ӷ������˼�ʽ�Ȼ�þ�������������ܣ���ʽ�Ȼ�þ���ڶ�����ɽṹ����ѧͨʽ�ɱ�ʾΪMgx��OH��yClzmH2O������2x��y��z=0��0��m��6����
����˼��չ��
��1����þ��ϡ���ᷴӦ��ʵ��ʱ��Ϊ�˲����Թ��г��ֻҰ�ɫ������þ��������_______��
��2����Ƭ��ͭƬ����ϡ�����в���������Ҳ����ͬ���ݴ��Ʋ�����Ļ�Ա�ͭ_____��