题目内容
【题目】某白色固体可能含有 BaC12(溶液显中性)、NaOH、Na2CO3、Na2SO4 中的一种或几种,某小组同学为确定该白色固体的成分,进行如下探究。
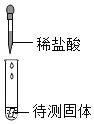
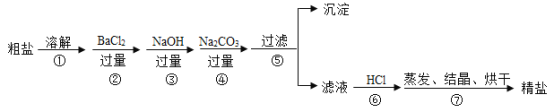
① 初步探究:实验设计如下图所示。
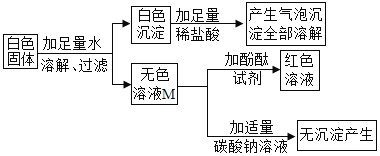
(初步结沦)原白色固体中一定有的物质是_____________,一定没有的物质是_____________。M溶液中的溶质一定有_____________,一定没有 BaCl2 ,理由是_____________(用化学方程式表示)
(交流讨论)甲同学认为:无色溶液 M 变红色,说明溶液 M 中含有碱性物质,但不能说明原白色固体中是否含有氢氧化钠,需要进一步确定。
② 继续探究:无色溶液 M 中是否含有氢氧化钠?
(实验探究)
实 验 步 骤 | 实 验 现 象 | 实 验 目 的 | 实验结论 |
A取溶液 M 于试管中,加入______,振荡,静置。 | 白色沉淀 | _______ | ______ |
B取实验 A 所得的上层清液于试管中,加入____试剂。 | _____ | 证明溶液 M 中是否有氢氧化钠 | 原白色固体中含有氢氧化钠 |
通过实验,小组同学完成了本次探究活动。
【答案】BaC12、Na2CO3 Na2SO4 NaCl ![]() 足量CaCl2溶液 除去溶液中可能剩余的Na2CO3 溶液M中存在Na2CO3 无色酚酞 无色溶液变红
足量CaCl2溶液 除去溶液中可能剩余的Na2CO3 溶液M中存在Na2CO3 无色酚酞 无色溶液变红
【解析】
[初步结沦]白色固体混合产生白色沉淀,说明一定存在氯化钡和碳酸钠或硫酸钠,白色沉淀和足量稀盐酸反应有气泡且沉淀全部溶解,说明白色沉淀成分是碳酸钡,而不是硫酸钡,则原白色固体中一定有的物质是氯化钡和碳酸钠,一定没有的物质是硫酸钠。M溶液中的溶质一定有氯化钡和碳酸钠反应的生成物氯化钠,一定没有BaCl2,理由是加适量碳酸钠无明显现象,若有氯化钡,则碳酸钠和氯化钡会发生反应,用化学方程式表示为![]() 。
。
[实验探究] 无色M溶液加酚酞变化,可能是有碳酸钠或氢氧化钠或碳酸钠和氢氧化钠,预想证明氢氧化钠存在与否,需要排除碳酸钠的干扰,可加中性溶液氯化钙溶液,可与碳酸钠反应生成沉淀,故填表如下:
实 验 步 骤 | 实 验 现 象 | 实 验 目 的 | 实验结论 |
A取溶液 M 于试管中,加入足量CaCl2溶液,振荡,静置。 | 白色沉淀 | 除去溶液中可能剩余的Na2CO3 | 溶液M中存在Na2CO3 |
B取实验 A 所得的上层清液于试管中,加入无色酚酞试剂。 | 无色溶液变红 | 证明溶液 M 中是否有氢氧化钠 | 原白色固体中含有氢氧化钠 |