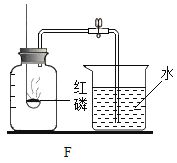
题目内容
【题目】从微观的角度来认识物质的构成和物质的变化,是学习化学的重要方法。
(1)下列物质中,由原子直接构成的是_____。
A 甲烷 B 金刚石 C 硫酸铜 D 氮气
(2)下图分别是物质发生变化的微观示意图。
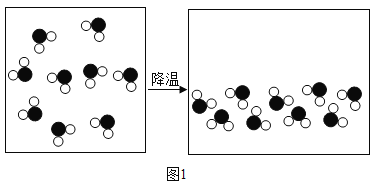
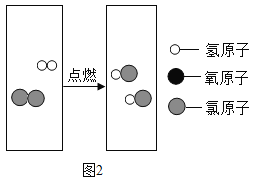
请回答:
①图1表示的变化,从微观角度看改变的是_____。
②图2表示的变化,所表示的宏观事实是(用文字表达)_____。
(3)工业上可以用一氧化碳还原四氧化三锰炼锰。1个四氧化三锰“分子”与_____个CO分子完全反应生成Mn和CO2.若用22.9t含四氧化三锰50%的锰矿石炼锰,理论上能炼得_____t金属锰。
【答案】B 分子间隔变小 氢气在氯气中燃烧产生氯化氢 4 8.25
【解析】
(1)
A、甲烷是由甲烷分子构成的;
B、金刚石是由碳原子构成的;
C、硫酸铜是由硫酸根离子和铜离子构成的;
D、氮气是由氮气分子构成的;
故选:B。
(2)①图1中没有新物质产生,表示物理变化,从微观角度看改变的是:水分子间的间隔变小;
②图2中有新物质产生,表示化学变化,所表示的宏观事实是:氢气在氯气中燃烧产生氯化氢;
(3)工业上可以用一氧化碳还原四氧化三锰炼锰。该反应符合质量守恒定律,每1个四氧化三锰“分子”与4个CO分子完全反应生成3个Mn原子和4个二氧化碳分子。
解:设论上能炼得金属锰为x。
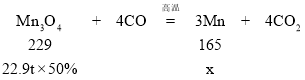
![]() x=8.25t;
x=8.25t;
理论上能炼得8.25t金属锰。

 阅读快车系列答案
阅读快车系列答案【题目】某白色固体可能含有 BaC12(溶液显中性)、NaOH、Na2CO3、Na2SO4 中的一种或几种,某小组同学为确定该白色固体的成分,进行如下探究。
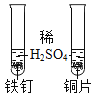
① 初步探究:实验设计如下图所示。
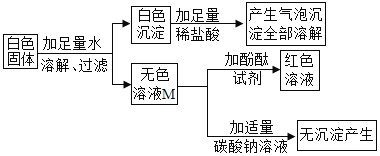
(初步结沦)原白色固体中一定有的物质是_____________,一定没有的物质是_____________。M溶液中的溶质一定有_____________,一定没有 BaCl2 ,理由是_____________(用化学方程式表示)
(交流讨论)甲同学认为:无色溶液 M 变红色,说明溶液 M 中含有碱性物质,但不能说明原白色固体中是否含有氢氧化钠,需要进一步确定。
② 继续探究:无色溶液 M 中是否含有氢氧化钠?
(实验探究)
实 验 步 骤 | 实 验 现 象 | 实 验 目 的 | 实验结论 |
A取溶液 M 于试管中,加入______,振荡,静置。 | 白色沉淀 | _______ | ______ |
B取实验 A 所得的上层清液于试管中,加入____试剂。 | _____ | 证明溶液 M 中是否有氢氧化钠 | 原白色固体中含有氢氧化钠 |
通过实验,小组同学完成了本次探究活动。
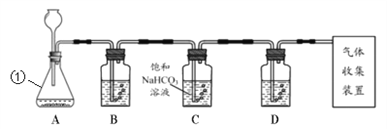
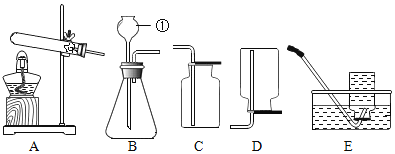
【题目】常温下没有氧气存在时,铁与水几乎不反应,但高温下,铁与水蒸气能反应生成一种常见的铁的氧化物和一种气体。小明很好奇,设计如图所示实验,探究铁粉与水蒸气反应后的产物。

(1)试管尾部放一团湿棉花的目的是_____。
(查阅资料)
(2)探究生成的气体是什么?
用燃着的木条靠近肥皂泡,有爆鸣声,稍后有肥皂泡飘到空中。说明生成的气体是_____。
(3)探究试管中剩余固体成分是什么?
常见铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
颜色、状态 | 黑色粉末 | 红棕色粉末 | 黑色晶体 |
能否被磁铁吸引 | 否 | 否 | 能 |
(初步验证)试管中剩余固体为黑色,能全部被磁铁吸引。该黑色固体不可能是_____。铁和水蒸气反应的化学方程式为_____。
(猜想与假设)猜想一:剩余固体是Fe与Fe3O4;猜想二:剩余固体是_____。
(查阅资料)![]() 。
。
(实验探究)小明继续进行实验探究。取该剩余固体少量于试管中,加入足量的稀盐酸,观察到_____现象,得出结论“猜想一成立”。