题目内容
【题目】实验室部分装置如图所示。请问答下列问题。
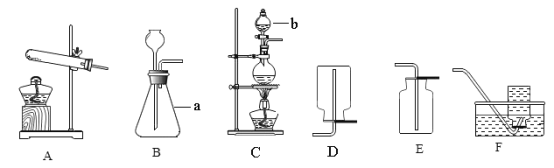
(1)写出仪器的名称a_______________,b_______________。
(2)实验室用高锰酸钾制取氧气时,选择的发生装置是_______________(填字母),该装置需要改进的地方是_______________,发生反应的化学方程式为_______________。
(3)实验室制取CO2的化学反应方程式为_______________,检验CO2的方法是_______________。
(4)实验室通过加热亚硝酸钠和氯化铵的混合溶液制取并收集N2时,应选择的发生装置是______________(填字母)。
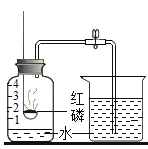
(5)下列实验装置是可用于制取检验并吸收SO2的创新实验装置。资料SO2气体具有漂白性,能使有色物质褪色。实验步骤如下:
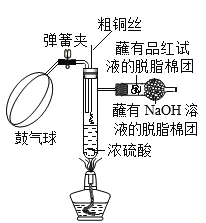
①将仪器按如图组装好,检查装置气密性,然后装入药品,固定在铁架台上,关闭弹簧夹;
②点燃酒精灯,用力下推粗铜丝,使螺旋状部分进入沸腾的浓硫酸中,反应立即开始,片刻后观察到蘸有品红溶液的脱脂棉团褪色;
③反应一段时间后, 将粗铜丝用力上提,反应立即停止。为减少管内残留的SO2气体对空气的污染接下来的实验操作是_______________。
④待具支试管内液体冷却后,可观察到试管底部有少量白色固体生成。取下橡胶塞和干燥管,将上层液体倒掉,并向管内白色固体中加入少量蒸馏水,得到蓝色溶液,由此可以判断,白色固体的化学式为_______________。
综合上述实验步骤和现象,请回答:制取SO2的化学方程式为_______________;该实验的主要优点为装置集成化、绿色环保、_______________。
【答案】锥形瓶 分液漏斗 A 在试管口塞一团棉花 ![]()
![]() 将气体通入澄清石灰水,澄清石灰水变浑浊,说明该气体为二氧化碳 C 打开弹簧夹,挤压鼓气球鼓入空气排出装置内的气体
将气体通入澄清石灰水,澄清石灰水变浑浊,说明该气体为二氧化碳 C 打开弹簧夹,挤压鼓气球鼓入空气排出装置内的气体 ![]()
![]() 可以控制反应的发生和停止
可以控制反应的发生和停止
【解析】
(1)仪器a的名称为锥形瓶,仪器b的名称为分液漏斗。
(2)实验室用高锰酸钾制取氧气时,高锰酸钾固体在加热条件下生成锰酸钾、二氧化锰和氧气,选择固固加热型发生装置,选择的发生装置是A,为了防止高锰酸钾颗粒进入导管造成堵塞,应该在试管口塞一团棉花,因此该装置需要改进的地方是在试管口塞一团棉花,发生反应的化学方程式为![]() 。
。
(3)实验室制取CO2的原理是碳酸钙与稀盐酸反应生成氯化钙、二氧化碳和水,反应的化学反应方程式为![]() ,检验CO2的方法是将气体通入澄清石灰水,澄清石灰水变浑浊,说明该气体为二氧化碳。
,检验CO2的方法是将气体通入澄清石灰水,澄清石灰水变浑浊,说明该气体为二氧化碳。
(4)实验室通过加热亚硝酸钠和氯化铵的混合溶液制取并收集N2时,应选择液体与液体反应并加热的发生装置,图中的装置C符合题意。
(5)由制取检验并吸收SO2的创新实验装置图和相关资料可知:
①将仪器按如图组装好,检查装置气密性,然后装入药品,固定在铁架台上,关闭弹簧夹;
②点燃酒精灯,用力下推粗铜丝,使螺旋状部分进入沸腾的浓硫酸中,反应立即开始,片刻后观察到蘸有品红溶液的脱脂棉团褪色;
③反应一段时间后,将粗铜丝用力上提,反应立即停止。为减少管内残留的SO2气体对空气的污染接下来的实验操作是打开弹簧夹,挤压鼓气球鼓入空气排出装置内的气体。
④待具支试管内液体冷却后,可观察到试管底部有少量白色固体生成。取下橡胶塞和干燥管,将上层液体倒掉,并向管内白色固体中加入少量蒸馏水,得到蓝色溶液,由此可以判断,白色固体为硫酸铜,硫酸铜溶解在水中溶液为蓝色,硫酸铜的化学式为![]() 。
。
综合上述实验步骤和现象可知铜和浓硫酸在加热条件下反应生成硫酸铜、二氧化硫和水,则制取SO2的化学方程式为![]() ;该实验的主要优点为装置集成化、绿色环保、可以控制反应的发生和停止。
;该实验的主要优点为装置集成化、绿色环保、可以控制反应的发生和停止。

 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案 全程金卷系列答案
全程金卷系列答案