题目内容
【题目】在学习酸的性质时,小红为了表示反应实质绘制下图,请结合图示回答问题:
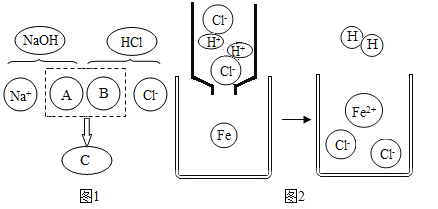
(1)常温下NaOH溶液的pH____7(填>、<、=)。
(2)图1描述了氢氧化钠溶液与盐酸反应的微观示意图,C为____(填化学式)。
(3)图2是表示盐酸加入到铁粉中,可观察到的现象是____;恰好完全反应时,所得溶液的溶是_____(填化学式)。
(4)在盐酸中滴加几滴紫色石蕊溶液,观察到的现象是_____;醋酸溶液也会使紫色石蕊溶液变色,原因是两溶液均含有一种相同的离子,该离子是____(填离子符号)。
【答案】> H2O 生成气泡,溶液由无色变为浅绿色 FeCl2 溶液变红 H+
【解析】
(1)常温下NaOH溶液的pH > 7,故填:>;
(2)图1描述了氢氧化钠溶液与盐酸反应的微观示意图,氢氧化钠是由钠离子和氢氧根离子构成,盐酸是由氢离子和氯离子构成,反应的微观实质是氢离子和氢氧根离子结合生成水分子,所以图中A、B、C处应填入的化学符号依次为OH-、H+、H2O。故填:H2O;
(3)图2是表示盐酸加入到铁粉中,可观察到的现象是生成气泡,溶液由无色变为浅绿色;恰好完全反应时,所得溶液的溶质是FeCl2故填:生成气泡;FeCl2
(4)石蕊遇酸性溶液会变红色,所以将紫色石蕊试液滴加到盐酸溶液中溶液变红;醋酸溶液也会使,紫色石蕊溶液变色,原因是两溶液均含有一种相同的离子,该离子是H+因此,故填:溶液变红;H+。

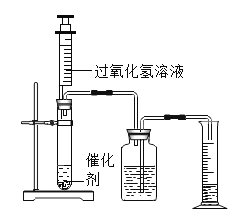
【题目】为了探究影响化学反应速率的因素,某化学兴趣小组的同学设计了如图所示的装置进行实验,收集的相关数据如下表:
实验序号 | H2O2溶液的浓度% | H2O2溶液的体积/mL | 催化剂/g | 温度/ | 收集相同体积的O2所需的时间/s |
① | 5 | 2 | 0.1gMnO2 | 20 | 18 |
② | 10 | 2 | 0.1gMnO2 | 20 | 6 |
③ | 30 | 8 | 未加 | 40 | 64 |
④ | 30 | 8 | 未加 | 60 | 25 |
⑤ | 10 | a | 0.1gCuO | b | 16 |
(1)过氧化氢溶液与二氧化锰反应的化学方程式____。
(2)由实验_____(填实验序号)知,化学反应速率与H2O2溶液的浓度有关;由实验③和④知,化学反应速率与温度的关系是_____。
(3)表中的数据还反映出不同的催化剂对双氧水溶液分解的催化效果不同,则表中的a=___,b=____
【题目】根据下列实验装置图,问答问题。

(1)写出标有序号的仪器名称:a__________,b_________。
(2)在实验室中用过氧化氢溶液和二氧化锰混合制取氧气时,发生反应的化学方程式为______,应选择的发生装置为_______。(填写装置的字母代号),若收集到的氧气不纯,可能的原因是______。(填序号)
①导管口一有气泡就马上收集
②装置漏气
③收集气体的集气瓶内未装满水
(3)若用 E 装置收集氧气,如何检验氧气已收集满? ______。
(4)小虎探究了影响双氧水分解速率的某种因素,实验数据记录如表:
双氧水的质量 | 双氧水的浓度 | MnO2的质量 | 相同时间内产生 O2的体积 | |
I | 50.0g | 1% | 0.1g | 9mL |
II | 50.0g | 2% | 0.1g | 16mL |
III | 50.0g | 4% | 0.1g | 31mL |
小虎的实验结论是:________。
(5)实验室常用加热无水醋酸钠与碱石灰固体混合物来制取甲烷气体。要制取并收集甲烷(密度比空气小,难溶于水),可选用的发生、收集装置依次是____。