题目内容
【题目】某校化学兴趣小组欲用4.9%的稀H2SO4,测定一瓶标签破损的NaOH溶液的溶质质量分数。
(1)欲配制100g4.9%的稀硫酸溶液,需用98%的浓硫酸_____g。
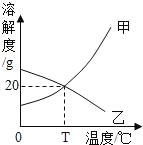
(2)取10gNaOH溶液样品与4.9%的稀硫酸溶液混合,溶液中pH变化如图所示。当加入稀硫酸质量小于20g时,混合溶液中的溶质为_____(填化学式)。

(3)NaOH溶液样品中溶质的质量分数为____。
【答案】5 Na2SO4和NaOH 8%
【解析】
(1)欲配制100g4.9%的稀硫酸溶液,根据稀释过程溶质的质量不变可得,需用98%的浓硫酸![]() =5g。
=5g。
(2)取10gNaOH溶液样品与4.9%的稀硫酸溶液混合,溶液中pH变化如图所示。当加入20g稀硫酸恰好完全反应,所以当加入稀硫酸质量小于20g时,此时氢氧化钠还有剩余,所以混合溶液中的溶质为生成的Na2SO4和剩余的NaOH。
(3)设NaOH溶液样品中溶质的质量分数为x,
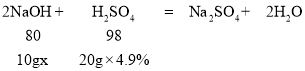
![]()
x=8%,NaOH溶液样品中溶质的质量分数为8%。

 灵星计算小达人系列答案
灵星计算小达人系列答案【题目】小明在学习金属活动性顺序后,知道钾、钙、钠的金属活动性特别强,能与水反应生成碱和氢气。他思考镁紧排在钠后面,那么它是否也能与水反应呢?
【提出问题】镁是否能与水反应?
【实验探究】在两个烧杯中,分别加入等量的冷水和镁条,用酚酞作指示剂。实验过程和现象如图:

【反思与总结】
(1)小明得出的实验结论是________________________________。
(2)小明发现B试管放置在空气中一会儿,溶液的红色会褪色,这说明溶液的碱性减弱了。
猜想 | 验证方案 |
可能是氢氧化镁的溶解度受温度的影响,温度降低,溶解度变小,从而导致溶液碱性减弱 | 将褪色的溶液________,如果溶液变红,说明小明的猜想正确 |
小明通过实验证明了自己的猜想是正确的。
(3)一段时间后,小明观察到镁条在热水中无现象,但当他想到实验室制取二氧化碳不能用稀硫酸与大理石反应时,便有了解释,他的解释是________________________________________________________________________。