题目内容
【题目】铝、铁、铜是我们生活中常见的金属。
(1)铝的利用比铜、铁晚是因为金属大规模开发和利用的先后顺序与_____(填字母)有关。
A 金属的活动性
B 金属的导电性
C 金属在底壳中的含量
(2)铝具有很好的抗腐蚀性能,原因是_____。
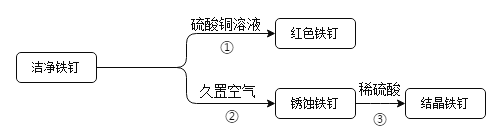
(3)化学新材料的应用,使人们的生活质量不断提高。如图是不同年代常用的水管。

①图示所有水管中,含有的金属元素是_____。
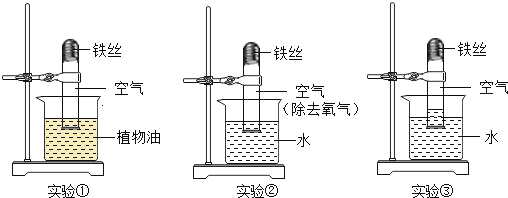
②每年全世界钢铁的产量很高,但钢铁的锈蚀也给人类带来了巨大的损失,铁在空气中锈蚀,实际上是铁跟_____共同作用的结果;工业上常用稀盐酸来除铁锈(Fe2O3),该反应的化学方程式是_____。请你提出一种防止铁制品锈蚀的方法:_____。
③铁丝在空气中不能燃烧却在氧气中剧烈燃烧,其燃烧的化学方程式为_____。
(4)印刷铜制电路板的“腐蚀性”为与FeCl3溶液反应,化学方程式分别为①Cu+2FeCl3===2FeCl2+CuCl2;②Fe+2FeCl3===3X。则②中X的化学式为_____。
【答案】(1)A;(2)铝表面有一层致密的氧化铝保护膜,从而阻止铝进一步被氧化;
(3)①Fe、Zn;②氧气( 或空气)和水;6HCl+Fe2O3=2FeCl3+3 H2O,在铁制品表面涂漆;
③3Fe+2O2![]() Fe3O4
Fe3O4
(4)FeCl2
【解析】
试题(1)地壳里含量最高的是金属铝,但铝开发利用的时间在铜和铁之后,说明金属大规模开发、利用的先后顺序与地壳里金属含量无关,与金属的导电性也无关。金属大规模开发利用主要和金属的活动性有关,活动性弱的金属容易以单质形式存在,易被开发和利用;活动性强的金属一般以化合物形式存在,有的还比较难冶炼;
(2)根据铝与空气中的氧气反应生成的氧化物的特点分析。铝具有很好的抗腐蚀性能,原因是铝表面有一层致密的氧化铝保护膜,从而阻止铝进一步被氧化;
(3)①根据水管中含有的金属元素回答。在水管中含有的金属元素有Fe、Zn;
②根据铁生锈的条件回答。铁在空气中锈蚀,实际上是铁跟氧气( 或空气)和水共同作用的结果,工业上常用稀盐酸来除铁锈(Fe203),该反应的化学方程式是6HCl+Fe2O3=2FeCl3+3 H2O;由铁生锈的条件可知防止铁生锈的措施有:在铁制品表面涂漆,保持铁制品表面的洁净干燥等;
③铁在氧气中燃烧生成了四氧化三铁,反应的方程式是:3Fe+2O2![]() Fe3O4;
Fe3O4;
(4)根据质量守恒定律反应前后原子的种类和数目不变分析在Fe+2FeCl3=3X的左边有铁原子3个,氯原子6个,由于反应前后原子的种类和数目不变,则每个X中含有一个铁原子和2个氯原子,所以化学式是:FeCl2。

【题目】水和溶液在生产、生活中起着十分重要的作用,请回答下列问题。
(1)自来水厂主要通过①沉淀②吸附③过滤④投药消毒(用漂白粉等)等对自然水进行净化,其合理的步骤顺序是_____(填序号);日常生活中可用_____的方法降低水的硬度。
(2)如图是超市里一种盐汽水的营养成分表。
营养成分表 | |||
项目 | 每100毫克 | 单位 | 营养素参考值% |
能量 | 43 | 千焦 | 1% |
蛋白质 | 0 | 克 | 0% |
脂肪 | 0 | 克 | 0% |
碳水化合物 | 25 | 克 | 1% |
钠 | 118 | 毫克 | 6% |
①该汽水含人体所需的六大营养素中的_____种。
②“钠118毫克”是指_____(填“钠单质”或“钠元素”)的质量。
③常温下打开该汽水瓶盖时,汽水会自动喷出来,这说明气体在水中的溶解度与_____有关。
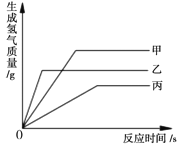
(3)如图是甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线,回答下列问题。
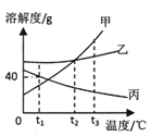
①t1℃时,将25g丙加入到50g水中充分溶解后所得溶液的质量为_____g。
②t2℃时,甲的溶解度_____(填“>”、“<”或“=”)乙的溶解度。
③甲中含有少量的乙,欲提纯甲应采用的方法是_____。
④将t3℃时甲、乙、丙三种物质的饱和溶液降温到t1℃时所得三种溶液溶质质量分数大小关系_____。