题目内容
【题目】常温下没有氧气存在时,铁与水几乎不反应,但高温下,铁与水蒸气能反应生成一种常见铁的氧化物和一种气体。小明很好奇,设计如下实验探究铁粉与水蒸气反应后的产物。

![]() 试管尾部放一团湿棉花的目的是_____。
试管尾部放一团湿棉花的目的是_____。
![]() 探究生成的气体是什么?
探究生成的气体是什么?
用燃着的木条靠近肥皂泡,有爆鸣声,稍后有肥皂泡飘到空中。说明生成的气体是_____。
![]() 探究试管中剩余固体成分是什么?
探究试管中剩余固体成分是什么?
(查阅资料)
常见铁的氧化物 | FeO |
|
|
颜色、状态 | 黑色粉末 | 红棕色粉末 | 黑色晶体 |
能否被磁铁吸引 | 否 | 否 | 能 |
(初步验证)试管中剩余固体为黑色,能全部被磁铁吸引。
(猜想与假设)猜想一:剩余固体是Fe与Fe3O4;猜想二:剩余固体是_____。
(实验探究)
实验操作 | 实验现象 | 结论 |
_____ | _____ | _____ |
(实验结论)铁和水蒸气反应的化学方程式为_____。
(反思与交流)该黑色固体不可能是Fe2O3,理由是_____。
【答案】提供水蒸气 氢气 Fe3O4 取少量黑色固体于试管中,加入足量的稀盐酸 固体全部溶解,没有气泡冒出或固体全部溶解,有气泡冒出 有气泡冒出,猜想一正确,或没有气泡冒出,猜想二正确 3Fe+4H2O![]() Fe3O4+4H2↑ Fe2O3是红棕色粉末且不能被磁铁吸引
Fe3O4+4H2↑ Fe2O3是红棕色粉末且不能被磁铁吸引
【解析】
(1)由题文可知,高温下,铁与水蒸气能反应,湿棉花中的水受热变为水蒸气,可以给铁提供水蒸气,故填提供水蒸气。
(2)用燃着的木条靠近肥皂泡,有爆鸣声,说明生成的气体具有可燃性,稍后有肥皂泡飘到空中,说明生成的气体的密度小于空气的密度,且反应物为“铁与水蒸气”,根据质量守恒定律可判断生成的气体是氢气,故填氢气。
(3){猜想与假设}能被磁铁吸引的物质只有Fe与Fe3O4,猜想一为Fe与Fe3O4,且反应后的固体不可能只有Fe没有其他生成物,所以猜想二是Fe3O4,故填Fe3O4。
{实验探究}实验操作:猜想乙与猜想二的区别是否含有铁,所以操作方法是取少量黑色固体于试管中,加入足量的稀盐酸,故填取少量黑色固体于试管中,加入足量的稀盐酸;
实验中的现象是固体全部溶解,没有气泡冒出,或者固体全部溶解,有气泡冒出,故填固体全部溶解,没有气泡冒出或固体全部溶解,有气泡冒出;
有气泡冒出,说明有氢气生成,表面固体中含有铁,则猜想一正确,如果没有气泡冒出,说明固体中不含铁,则猜想二正确,故填有气泡冒出,猜想一正确,或没有气泡冒出,猜想二正确。
{实验结论}由高温下,铁与水蒸气能反应生成一种常见铁的氧化物和一种气体及以上分析可知,铁与水蒸气在高温的条件下反应生成四氧化三铁和氢气,故反应的化学方程式写为:3Fe+4H2O![]() Fe3O4+4H2↑。
Fe3O4+4H2↑。
{反思与交流}反应后试管中剩余固体为黑色,能全部被磁铁吸引,而Fe2O3是红棕色粉末且不能被磁铁吸引,所以反应后的黑色固体不可能是Fe2O3,故填Fe2O3是红棕色粉末且不能被磁铁吸引。

【题目】某化学兴趣小组为了分析生铁中铁的含量,进行了实验研究,即取60g经粉碎后的生铁,把800稀硫酸分4次加入到该样品中,测得数据记录如下表:
第1次 | 第2次 | 第3次 | 第4次 | |
加入稀硫酸质量(g) | 200 | 200 | 200 | 200 |
剩余固体质量(g) | 37.6 | 15.2 | 4 | 4 |
(说明:生铁中杂质不溶于水,也不与硫酸反应.)
(1)第2次测得剩余固体质量为15.2g,其成分为_____.
A 铁 B 铁和碳 C 碳
(2)生铁中铁的质量分数为多少?(写出计算过程,结果保留到小数点后一位)_____
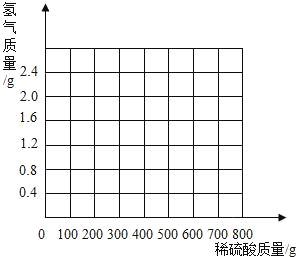
(3)计算所用稀硫酸的溶质质量分数为多少?_____(写出计算过程,结果保留到小数点后一位)并画出反应生成的氢气质量与加入稀硫酸质量的关系图._____