题目内容
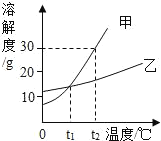
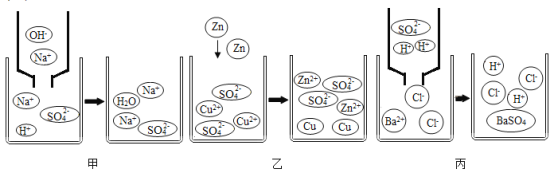
【题目】向盛有稀硫酸和硫酸铁的混合液的烧杯中加入某浓度的氢氧化钠溶液,产生沉淀的质量与加入氢氧化钠溶液的质量关系如图所示。下列分析正确的是
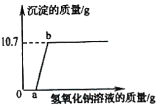
A. 向oa段(不含a点)溶液中滴入紫色石蕊试液变红
B. 到达b点时,烧杯内的溶液中含有两种溶质
C. 到达b点时,所消耗氢氧化钠溶液中溶质的质量是12g
D. 整个变化过程烧杯内的溶液中硫酸根离子数目没有改变
【答案】AD
【解析】
A. oa段(不含a点)是滴入的氢氧化钠溶液与稀硫酸反应,oa段(不含a点)溶液中含有稀硫酸,溶液显酸性,滴入紫色石蕊试液变红,此选项正确;
B. 到达b点时,稀硫酸与氢氧化钠溶液、硫酸铁恰好反应,烧杯内的溶液中只含有生成的硫酸钠一种溶质,此选项错误;
C. 设与硫酸铁反应的氢氧化钠溶液中溶质的质量为x,
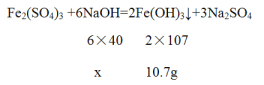
![]() =
=![]() ,解得x=12g
,解得x=12g
到达b点时,所消耗氢氧化钠溶液中溶质的质量是与稀硫酸和与硫酸铁反应的氢氧化钠溶液中溶质质量之和,>12g,此选项错误;
D. 该化学反应过程中,硫酸根离子作为一个整体参加反应,整个变化过程中硫酸根离子数目没有改变,此选项正确。故选AD。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】某化学兴趣小组在实验室里探究某些酸、碱、盐之间是否发生复分解反应。请你参与探究并填空:
(查阅资料)①硫酸铜和氯化铜的溶液都有毒。铜离子可以使蛋白质变性,可以杀死细菌和病毒,可以破坏人体细胞。②硫酸钠溶液呈中性,无毒。
(实验与探究)
内容 | 现象 | 实验解析 | 结论 | |
实验一 | 取少量稀盐酸于小试管中,滴入数滴碳酸钠溶液,振荡 | _____ | 化学方程式: Na2CO3+2HCl==2NaCl+H2O+CO2↑ | 生成物中有____或有____或有____生成时,复分解反应可以发生。 |
实验二 | 取少量氢氧化钠溶液于小试管中,滴入几滴酚酞试液振荡,液体呈现红色;再滴入足量的稀硫酸 | _____ |
| |
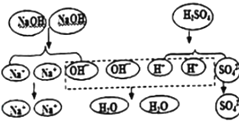
实验三 | 取少量氯化铜溶液于小试管中,滴入几滴氢氧化钠溶液试液,振荡 | _____ | 该反应的微观实质是:______; |
(废液处理)实验结束时,老师指出,废液定要进行无害化处理,尽量实现绿色排放(不考虑酚酞试液)。同学们把三个实验的试管内所有物质都倒入一个洁净的烧杯中得到蓝色澄清液体。根据上述现象,同学们向废液中逐滴滴加_____溶液,直至观察到_____。说明废液达到了绿色排放的要求。
【题目】常温下没有氧气存在时,铁与水几乎不反应,但高温下,铁与水蒸气能反应生成一种常见铁的氧化物和一种气体。小明很好奇,设计如下实验探究铁粉与水蒸气反应后的产物。
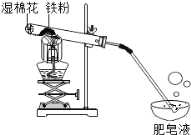
![]() 试管尾部放一团湿棉花的目的是_____。
试管尾部放一团湿棉花的目的是_____。
![]() 探究生成的气体是什么?
探究生成的气体是什么?
用燃着的木条靠近肥皂泡,有爆鸣声,稍后有肥皂泡飘到空中。说明生成的气体是_____。
![]() 探究试管中剩余固体成分是什么?
探究试管中剩余固体成分是什么?
(查阅资料)
常见铁的氧化物 | FeO |
|
|
颜色、状态 | 黑色粉末 | 红棕色粉末 | 黑色晶体 |
能否被磁铁吸引 | 否 | 否 | 能 |
(初步验证)试管中剩余固体为黑色,能全部被磁铁吸引。
(猜想与假设)猜想一:剩余固体是Fe与Fe3O4;猜想二:剩余固体是_____。
(实验探究)
实验操作 | 实验现象 | 结论 |
_____ | _____ | _____ |
(实验结论)铁和水蒸气反应的化学方程式为_____。
(反思与交流)该黑色固体不可能是Fe2O3,理由是_____。