题目内容
【题目】在学习了空气中氧气含量测定后,李老师给同学们布置了一道作业题:根据已有知识再设计几套测定空气中氧气含量的装置。以下是同学们设计的装置中的三套。

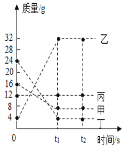
实验甲:先将红磷点燃后伸入集气瓶,待装置冷却再打开止水夹;
实验乙:先在试管中放入一团白磷,用橡皮塞塞紧后放入热水中,使白磷燃烧,待装置冷却后将试管如图乙倒立于水槽中,并在水下取下橡皮塞;
实验丙:在一个带有活塞和刻度的容器内放入一团白磷(白磷的着火点很低只有40度),置于盛有80度热水的烧杯上方。
(1)从环保的角度分析,甲和乙哪一个装置更好?__________。
(2)小丽同学按照丙装置进行实验,她观察到白磷_________,活塞先往________(填“左”或“右”)移,最后活塞停留在_________刻度处。请写出该实验的文字表达式________________。
【答案】乙 剧烈燃烧,产生大量白烟,放出大量的热 右 8 ![]()
【解析】
(1)使用甲装置测定空气中氧气的含量时,需在检查装置的气密性后,将燃烧匙从集气瓶中拿出来,放入红磷,在酒精灯上引燃红磷后,再将燃烧匙迅速伸入集气瓶内。而乙装置实验过程中不需要打开装置,从环保的角度分析,甲和乙相比,乙装置更好,因为生成的五氧化二磷不会逸散到空气中,不会污染环境;
(2)按照丙装置进行实验,观察到白磷剧烈燃烧,产生大量白烟,放出大量的热,使装置内气压增大,活塞先往右移动,后向左移动,因为氧气约占空气体积的五分之一,最后活塞停留在8刻度处。该实验的文字表达式![]() 。
。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】实验室提供下列药品:碳酸钠固体、块状大理石、粉末状大理石、稀硫酸、稀盐酸和浓盐酸;A、B、C、D、E、F、G、H等装置和试管等仪器.
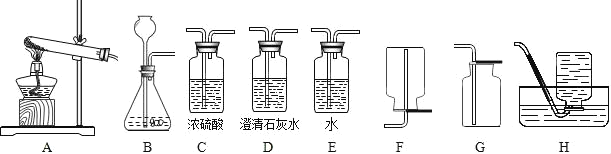
(1)制取CO2的发生装置选_____(填序号),按要求连接好装置后,在装入药品之前必不可少的操作_____.制CO2的装置还可以用来制取_____气体,其反应原理是:_____(用化学方程式表示).将装置A和装置H连接可制取我们常见的_____气体.
(2)检验二氧化碳的方法用化学方程式表示为_____.
(3)在四支试管中取等量固体和稀硫酸、稀盐酸反应,现象如表.
反应物 | ①粉末状大理石 +稀盐酸 | ②碳酸钠固体 +稀硫酸 | ③块状大理石 +稀盐酸 | ④块状大理石 +稀硫酸 |
现 象 | 剧烈,瞬间完成 | 剧烈,瞬间完成 | 有平稳气流产生 | 很慢,稍后停止 |
由此推知,实验室用于制取CO2的药品最合理的是_____(填序号);该反应的反应方程式为:_____.
(4)若要制取干燥的CO2,所有装置的连接顺序为_____.
(5)若不慎用浓盐酸代替稀盐酸制得了CO2气体,要得到纯净干燥的CO2,所有装置的连接顺序为_____.