题目内容
【题目】以下是实验室配制一定质量分数的氯化钠溶液的操作过程示意图。
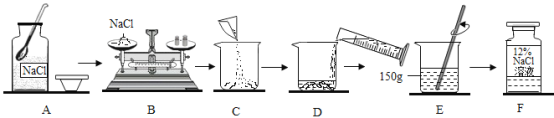
请根据示意图回答:
(1)上述操作中,有错误的是_______(填字母序号)。
(2)通过计算可知,托盘天平左盘中固体氯化钠的质量为_______g。
(3)操作E中,玻璃棒的操作是_______,此操作的目的是______。
【答案】A 18 搅拌 加速溶解
【解析】
(1)上述操作中,有错误的是A,因为取药品时瓶塞要倒放在桌面上,防止污染试剂。故填:A。
(2)由图中E、F的数据显示,该实验目的是要配置150g质量分数为12%的氯化钠溶液,根据溶质质量=溶液质量×溶质的质量分数,需要氯化钠的质量为:![]() ,需要称量18g氯化钠 。故填:18。
,需要称量18g氯化钠 。故填:18。
(3)操作E是溶解操作,其中玻璃棒的操作是搅拌,目的是加速溶解。故填:搅拌;加速溶解。

 阅读快车系列答案
阅读快车系列答案【题目】在一次化学实验中,两组同学都完成了硫酸铜溶液与氢氧化钠溶液反应的实验,但观察到了不同的实验现象。
(进行实验一)
实验组 | 甲组 | 乙组 |
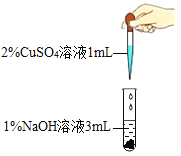
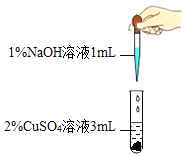
实验操作 |
|
|
实验现象 | 产生蓝色沉淀 | 产生蓝绿色沉淀 |
已知蓝色沉淀是氢氧化铜,写出生成蓝色沉淀的化学方程式_____。
(提出问题)乙组产生的蓝绿色沉淀的成分是什么呢?
(查阅资料)
(1)碱式硫酸铜是绿色晶体,在水中溶解度极小,能溶于稀酸溶液。
(2)碱式硫酸铜的组成不固定,一般可用Cu2(OH)2SO4表示。
(3)BaCl2溶液和含有SO42-的溶液反应能生成BaSO4(白色沉淀)。例如:BaCl2+H2SO4=BaSO4↓+2HCl
(猜想与假设)蓝绿色沉淀是碱式硫酸铜。
(进行实验二)
实验步骤 | 主要实验操作 | 现象及结论 |
① | 取乙组实验后的混合物过滤 | 得到蓝绿色沉淀 |
② | 取蓝绿色沉淀,用蒸馏水洗涤多次 | 无明显现象 |
③ | 向最后一次洗涤液中滴加BaCl2溶液 | 无沉淀产生 |
④ | 取洗涤后的蓝绿色沉淀于试管中,滴加稀盐酸 | 沉淀全部溶解,得到蓝绿色溶液 |
⑤ | 取少量蓝绿色溶液于试管中,滴加… | 产生白色沉淀 |
实验结论:蓝绿色沉淀是碱式硫酸铜 | ||
(解释与结论)
(1)步骤③的实验目的是_______。
(2)步骤④中的稀盐酸能否用稀硫酸代替?________。
(3)步骤⑤滴加的试剂是________。
(反思与评价)
(4)甲组同学在本组实验的基础上进一步完成下列实验:
①过滤,取蓝色沉淀于试管中
②滴加________,沉淀颜色变为蓝绿色
③重复实验二中的步骤①~⑤
经实验验证,氢氧化铜也可以转化为碱式硫酸铜。此反应的化学方程式为________。
(5)乙组同学认为在自己组原有实验的基础上,继续滴加_______,可以将碱式硫酸铜转变为氢氧化铜。通过实验,也验证了他们的猜想。
(6)为了确保氢氧化钠溶液和硫酸铜溶液反应生成氢氧化铜,实验的关键是_______。