题目内容
【题目】KNO3 和 KCl 在不同温度时的溶解度如表所示。请回答下列问题:
温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 |
KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 |
KCl | 27.6 | 31.0 | 34.0 | 37.0 | 40.0 | 42.6 | 45.5 | 48.3 |
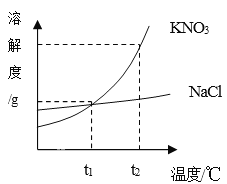
(1)依据上表数据,绘制 KNO3 和 KCl 的溶解度曲线,如图 1 中能表示 KNO3 溶解度曲线的是_____(填 m 或 n)。

(2)20 ℃时,向 10 g 水中加入 2.5 g KNO3 充分搅拌得到 X,再加入 2.5 g KNO3 充分搅拌得到 Y,继续升温至 50 ℃得到 Z,则 X、Y、Z 中为饱和溶液的是_____。
(3)40 ℃时,100 g 水中的硝酸钾饱和溶液稀释成溶质质量分数为10%的溶液,应加水的质量为_____。
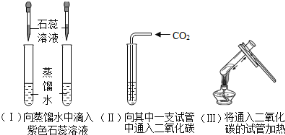
(4)如图 2 所示,20 ℃时,将盛有饱和 KNO3 溶液的小试管放入盛水的烧杯中,向水中加入某物质后,试管中有晶体析出。加入的物质可能是下列中的_____(填字母序号)。
A. 硝酸铵固体 B. 生石灰固体 C. 冰块
(5)将40℃时硝酸钾和氯化钾的饱和溶液,降温至10
A. KNO3溶液析出晶体的质量比KCl析出晶体的质量大
B. 在20℃和30℃之间某一温度,两种溶液的质量分数相等
C. 两种溶液的溶剂质量不变
D. 若继续对两溶液降温,则两溶液将会继续析出晶体,且水溶液会成为纯净物
【答案】m Y 475.1g AC BC
【解析】
(1)根据表格中数据可知,硝酸钾的溶解度受温度影响较明显,所以图 1 中能表示KNO3 溶解度曲线的是m。故填:m。
(3)20 ℃时,硝酸钾的溶解度为31.6g,即100g水中可以溶解31.6g硝酸钾达到饱和,所以 10 g水中最多可以溶解3.16g硝酸钾,向10g水中加入 2.5 g KNO3 充分搅拌得到 X为不饱和溶液,再加入 2.5 g KNO3 ,一共加入了5g硝酸钾,不能全部溶解,所以充分搅拌得到 Y是饱和溶液,继续升温至 50 ℃,该温度下硝酸钾的溶解度为85.5g,100g水中最多溶解85.5g达到饱和,10g水中可以溶解8.55g达到饱和,但是加入的硝酸钾只有5.0g,所以得到的Z为不饱和溶液,所以则X、Y、Z 中为饱和溶液的是Y。故填:Y。
(3)40 ℃时,100 g 水中的硝酸钾的饱和溶液(含溶质63.9g)稀释成溶质质量分数为10%的溶液,稀释后稀溶液的质量为![]() ,原溶液的质量为
,原溶液的质量为![]() ,所以应加水的质量为
,所以应加水的质量为![]() 。故填:475.1g。
。故填:475.1g。
(4)如图 2 所示,20 ℃时,将盛有饱和KNO3溶液的小试管放入盛水的烧杯中,向水中加入某物质后,试管中有晶体析出,温度降低会导致饱和硝酸钾溶液溶解度减小而析出晶体,所以加入的物质会导致溶液温度降低,符合题意的是A 硝酸铵固体(它溶解吸热,使溶液温度降低)或者C冰块(它要融化吸热,使溶液温度降低),但是B生石灰遇水反应放热,会使溶液温度升高,硝酸钾不会析出晶体。故选AC。
(5)A. 因为没有指明饱和硝酸钾溶液和饱和氯化钾溶液的质量是否相等,所以KNO3溶液析出晶体的质量与 KCl 析出晶体的质量无法比较。故A不符合题意;
B. 因为在20℃时氯化钾的溶解度大于硝酸钾的溶解度,在30℃时硝酸钾的溶解度大于氯化钾的溶解度,所以二者溶解度相等的温度点出现在20℃和30℃之间某一温度,将40℃时硝酸钾和氯化钾的饱和溶液,降温至 10℃,降温过程溶液始终饱和,当溶解度相等时两种溶液的质量分数相等为![]() 。故B符合题意;
。故B符合题意;
C. 将40℃时硝酸钾和氯化钾的饱和溶液,降温至 10℃,降温过程两种溶液只是会析出晶体,溶剂的质量不变。故C符合题意;
D. 若继续对两溶液降温,则两溶液将会继续析出晶体,但是水溶液不会成为纯净物,还会有少量晶体溶解在水中,溶液属于混合物。故D不符合题意。
故选BC。

 阅读快车系列答案
阅读快车系列答案