题目内容
【题目】如图所示,“五环”中相交两环中的物质间能够发生化学反应。
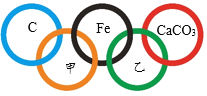
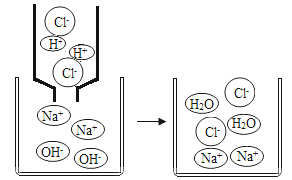
(1)甲、乙分别是氧气、氧化铁、稀盐酸、氢氧化钙四种物质中的一种,物质甲为______________________(填化学式),构成物质甲的微粒符号为:______________________,物质乙为_____________(填名称),构成物质乙的微粒的符号为__________________________。
(2)这五种物质中能发生置换反应的化学方程式是:_________________;物质甲与铁反应的化学方程式是:____________从赤铁矿中冶炼铁,用化学方程式表示:_____________。
(3)“五环” 中的物质Fe可以替换成_____________(填一种即可)。
【答案】O2 O2 稀盐酸 H+、Cl- H2O Fe+2HCl═FeCl2+H2↑ 3Fe+2O2![]() Fe3O4 Fe2O3+3CO
Fe3O4 Fe2O3+3CO![]() 2Fe+3CO2 Mg或者Al
2Fe+3CO2 Mg或者Al
【解析】
(1)甲、乙分别是O2、Fe2O3、稀盐酸、Ca(OH)2四种物质中的一种,铁和碳酸钙会与稀盐酸反应,所以乙是稀盐酸,氧气会与铁、碳反应,所以甲是氧气,经过验证,推导正确,所以甲物质为氧气,氧气由氧气分子构成,乙是稀盐酸,稀盐酸是混合物, 构成物质乙的微粒是氢离子、氯离子、水分子。
故填:O2;O2;稀盐酸;H2O、H+、Cl-;
(2)铁和稀盐酸反应生成氯化亚铁和氢气,反应的方程式为:Fe+2HCl═FeCl2+H2↑,该反应是置换反应;物质甲与铁反应是氧气和铁在点燃条件下生成四氧化三铁,反应的化学方程式是:3Fe+2O2![]() Fe3O4;用赤铁矿在高炉中冶炼铁的化学原理为Fe2O3+3CO
Fe3O4;用赤铁矿在高炉中冶炼铁的化学原理为Fe2O3+3CO![]() 2Fe+3CO2;
2Fe+3CO2;
故填:Fe+2HCl═FeCl2+H2↑;3Fe+2O2![]() Fe3O4;Fe2O3+3CO
Fe3O4;Fe2O3+3CO![]() 2Fe+3CO2;
2Fe+3CO2;
(3)“五环”中的物质Fe既可以在氧气燃烧也可以和稀盐酸反应,所以为 Mg或者Al(或其它合理答案)。故填:Mg或者Al。

【题目】长久使用热水壶底部有层水垢,主要成分为CaCO3和Mg(OH)2,某学校化学研究小组的同学通过实验测定水垢中CaCO3的含量:将过量的稀盐酸加入到200g水垢中,把产生的CO2气体用足量的NaOH溶液吸收,同时测量3min钟内NaOH溶液增加的质量,结果如下表:
时间/s | 0 | 30 | 60 | 90 | 120 | 150 | 180 |
质量/g | 0 | 30 | 50 | 60 | 66 | 66 | 66 |
(1)写出CO2被足量的NaOH溶液吸收时,发生的化学反应方程式_______________。
(2)从表格中可以看出,200g水垢与盐酸反应生成的CO2最多是___________g。
(3)计算水垢中碳酸钙的质量分数,写出计算过程_________