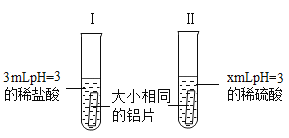
题目内容
【题目】2019 年 3 月 22 日是第二十七届“世界水日”。
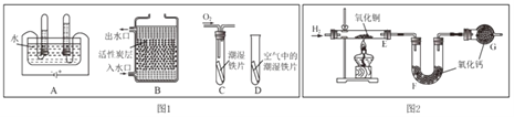
(1)根据图 1 回答下列问题。
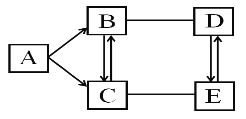
①A 图所示的是电解水实验,写出该反应的化学方程式______;
②B 图所示的是活性炭净水器的示意图,其中活性炭的作用是______。
③C、D 图所示的是探究铁生锈条件的实验,一段时间后发现 C 中铁片变红,D 中铁片依 然光亮,对比 C、D 中的现象,说明影响铁生锈快慢的一个重要因素是______。
(2)若用质量分数为 10%的氢氧化钠溶液(密度为 1.1g/cm3)配制 220g 质量分数为 5%的 氢氧化钠溶液。
①需要 10%的氢氧化钠溶液体积为______mL。
②实验室配制该溶液的主要步骤有:计算、量取、______、装瓶并贴上标签。
③若量取氢氧化钠溶液读数时仰视,而其余操作均正确,这样配得的溶液的溶质质量分数 会______(填“偏高”、“偏低”或“无影响”)。
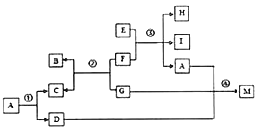
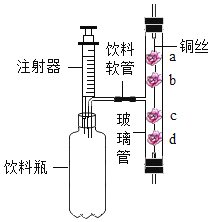
(3)根据上图 2 实验装置测定水的组成。 反应前后测得的 E、F 装置质量数据见表。
装置 E | 装置 F | |
反应前的质量/g | 38.2 | 212.4 |
反应后的质量/g | a | 214.2 |
①若测定水中氢、氧元素的质量比符合理论值,则表中 a 的数值是______。
②下列因素中,对测定结果有影响的是______(填字母)。
ACuO 粉末不干燥 BCuO 没有完全转化为 Cu C没有 G 装置
【答案】2H2O![]() 2H2↑+O2↑ 吸附 氧气的浓度 100 溶解 偏低 36.6 AC
2H2↑+O2↑ 吸附 氧气的浓度 100 溶解 偏低 36.6 AC
【解析】
(1)①根据水电解生成氧气和氢气进行分析解答;
②根据活性炭具有吸附性进行分析解答;
③根据铁生锈的条件进行分析解答;
(2)根据溶液配制的注意事项、有着溶质的质量分数的计算进行分析解答;
(3)①根据质量守恒定律和化学式的计算进行分析解答;
②根据影响测定结果的因素进行分析解答。
(1)①水通电生成氢气和氧气,化学方程式为:2H2O![]() 2H2↑+O2↑;
2H2↑+O2↑;
②B 图所示的是活性炭净水器的示意图,其中活性炭的作用是吸附;
③通过题干中信息可知,说明影响铁生锈快慢的一个重要因素是氧气的浓度;
(2)设需要 10%的氢氧化钠溶液的质量为x
![]() ,则x=110g
,则x=110g
110g10%氢氧化钠溶液的体积为:![]()
①需要 10%的氢氧化钠溶液体积为100mL;
②实验室配制该溶液的主要步骤有:计算、量取、溶解、装瓶并贴上标签;
③若量取氢氧化钠溶液读数时仰视,会使实际量取的液体体积比要量取的液体体积偏大,配制的溶液溶质的质量分数偏低;
(3)①生成水的质量![]()
装置 E反应后的质量为:![]()
②A 氧化铜不干燥,导致测定生成水的质量偏大,从而影响实验结果,选项A正确;
B 玻璃管中的氧化铜没有完全反应,不影响生成水的质量和减少的氧元素质量比,对测定结果无影响,选项B错误;
C 缺少G装置,导致测定生成水的质量偏大,从而影响实验结果,选项C正确。
故填:AC。

【题目】下列实验设计不能达到实验目的是( )
编号 | A | B | C | D |
实验设计 |
|
|
|
|
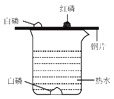
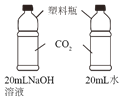
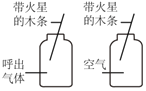
实验 目的 | 探究同种物质在不同 溶剂中的溶解性 | 探究物质燃烧的 条件 | 探究CO2与NaOH 发生反应 | 探究呼出气体与空气 中氧气含量的不同 |
A.AB.BC.CD.D
【题目】一定条件下,在一个密闭容器内发生某反应,测得反应前后各物质的质量如下表所示。
物质 | 甲 | 乙 | 丙 | 丁 |
反应前的质量/ | 10 | 10 | 10 | 2 |
反应前的质量/ | X | 2 | 21 | 2 |
A.X的值为4B.丙一定是化合物C.丁一定是催化剂D.该反应是分解反应