题目内容
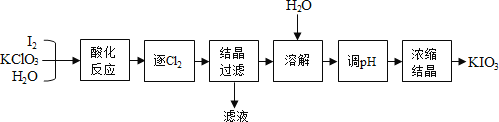
【题目】碘酸钾(KIO3)是一种重要的无机化合物,可作为食盐中的补碘剂。氯气(Cl2)常温常压下是一种黄绿色的气体,具有强氧化性。利用“KClO3 氧化法”制备KIO3工艺流程如下图所示:
请回答下列问题
(1)分别写出下列物质中氯元素的化合价:Cl2________;KC1O3_____________;
(2)“酸化反应”所得产物有KH(IO3)2、Cl2和KCl,可推测该反应中使用的酸是__________
(填名称);“逐Cl2”最简单的物理方法是_______;“结晶”后析出的晶体是KH(IO3)2,则“滤液”的主要成分除KH(IO3)2外还含有_____;“调pH”时需加入适量的KOH,请推测该过程中发生反应的化学方程式为______。
【答案】0 +5 盐酸 加热(或煮沸) KCl(或KCl、稀HCl) KH(IO3)2+KOH=2KIO3 +H2O
【解析】
⑴Cl2是单质,Cl2中氯元素的化合价为0;根据化合物中元素化合价代数和为0,KC1O3中氯元素化合价为+5;
⑵根据“酸化反应”所得产物有KH(IO3)2、Cl2和KCl,氯元素增加了,可推测该反应中使用的酸是盐酸;因为Cl2 是气体,气体的溶解度随温度的升高而减小,所以“逐Cl2”最简单的物理方法是加热(或煮沸);“结晶”后析出的晶体是KH(IO3)2,KCl没有析出故“滤液”的主要成分除KH(IO3)2外还含有KCl(或KCl、稀HCl);KH(IO3)2 转变为KIO3时,要反应掉其中的氢离子,同时不能带进新杂质,故 “调pH”时需加入适量的KOH,该过程中发生反应的化学方程式为KH(IO3)2+KOH=2KIO3 +H2O。

 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案【题目】I下图为实验室制取并收集氧气的部分装置图,据图回答:

(1)写出编号a的仪器名称_______
(2)若用B装置制取O2写出对应的化学反应方程式_____
(3)若用D(装满水)收集O2,则气体应从____(“b”或“c”)端导人。
Ⅱ小军同学在实验室帮老师整理药品时发现NaOH溶液试剂瓶口有一些白色固体,于是生好奇心:这白色固体是什么?他为此进行了如下探究
(查阅资料)①NaOH在空气中变质不会生成NaHCO3;
②CO2不溶解于饱和NaHCO3溶液中,也不与NaHCO3反应;
③Fe(OH)3呈红褐色,难溶于水;BaCl2溶液呈中性。
(提出猜想)猜想一:是NaOH猜想二:是Na2CO3猜想三:___
(实验探究)小军进行了下列实验探究
实验操作 | 实验现象 | 实验结论 |
①取少量白色固体于试管中,加水溶解,再加入足量BaCl2溶液 | __ | 猜想二正确 |
②过滤,在滤液中加入FeCl3溶液 | 无红褐色沉淀生成 |
(问题分析)实验操作①中加入足量BaCl2溶液的作用是______,实验操作②还有其他实验方案吗?如有,请写出一种实验方案(必须指明试剂和现象)_____
为了提高实验结论的准确性,小军又设计了如右图所示的实验对该白色固体的性质进行进一步探究:
(实验现象)A中有大量气泡产生,C中实验现象是______

(实验结论)白色固体是Na2CO3
(分析与反思)小军在与老师进行交流后得知,自己所设计的实验存在一定的缺陷,他对自己实验中存在的问题进行了反思:装置B中也能产生CO2。写出装置B中产生CO2的化学反应方程式____。改进措施:将浓盐酸换为稀盐酸。