题目内容
【题目】“5G”改变生活,中国芯彰显中国“智”造。芯片的基材主要是高纯硅,下图是一种制备高纯硅的工艺流程图:
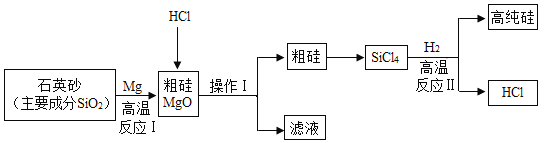
(1)反应1:镁在反应中作_____剂。
(2)操作I:操作名称是_____。
(3)反应II:发生反应的化学方程式为_____。该反应要在无氧气的环境中进行,原因是_____。(答出一种即可)。
(4).上述已知生产流程中,可以循环利用的物质是_____。
【答案】还原 过滤  防止氢气高温时发生爆炸 HCl
防止氢气高温时发生爆炸 HCl
【解析】
(1)反应1:镁得到氧元素形成氧化镁,在反应中作还原剂。
(2)操作I:将固体和液体分离的操作名称是:过滤;
(3)反应II:氢气与四氯化硅高温条件发生反应产生硅和氯化氢的化学方程式为: 。氢气具有可燃性,该反应要在无氧气的环境中进行,原因是:防止氢气高温时发生爆炸
。氢气具有可燃性,该反应要在无氧气的环境中进行,原因是:防止氢气高温时发生爆炸
(4)上述已知生产流程中,反应Ⅱ中产生的氯化氢正好是反应Ⅰ中原料,可以循环利用的物质是:HCl;

练习册系列答案
相关题目
【题目】草木灰是农村常用的一种肥料(其有效成分是K2CO3外)。某兴趣小组为了测定草木灰中K2CO3外的含量,取现有的草木灰40g放入锥形瓶中,将40g盐酸分4次(每次10g)加入瓶中,所得溶液总质量与加入盐酸的关系如下表;已知K2CO3+2HCl=2KCl+H2O+CO2↑(假设草木灰中除K2CO3外,其它物质均不溶于水,也不与盐酸反应)
所加次数 | 第一次 | 第二次 | 第三次 | 第四次 |
锥形瓶中物质总质量/g | 49.68 | 59.36 | 69.12 | 79.12 |
(1)以上四次实验,其中盐酸有剩余的是_____。
(2)第一次加入盐酸后产生气体的质量为_____克。
(3)草木灰中K2CO3的质量分数为多少_____?