题目内容
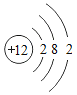
【题目】(1)某化学反应的微观示意图如下所示,据图回答问题:

丙分子中硫原子和氧原子的质量比是_____,请写出这个反应符号表达式_____。
(2)有下列物质:
①雨水;②蒸馏水;③雨后洁净的空气;④四氧化三铁;⑤液氮;⑥高锰酸钾完全分解后的固体产物。其中属于纯净物是_____,属于单质的是_____,属于氧化物的是_____。
【答案】![]()
![]() ②④⑤ ⑤ ②④
②④⑤ ⑤ ②④
【解析】
(1)丙分子的化学式为SO2,,硫原子和氧原子的质量比是32:(16×2)=1:1;由反应的微观示意图可知该反应是硫化氢与氧气反应生成了水和二氧化硫,反应的化学方程式是:H2S+O2→H2O+SO2;
故填:1:1;![]() 。
。
(2)雨水、空气中都含有多种物质,是混合物,高锰酸钾完全分解后的固体产物为锰酸钾和二氧化锰,也是混合物;蒸馏水中只有水一种物质,属于纯净物,且只有两种元素组成其中一种为氧元素,属于氧化物;四氧化三铁由两种元素组成的纯净物,其中一种为氧元素,属于氧化物;液氮只有一种元素组成的纯净物,属于单质。
故填:②④⑤;⑤;②④。

 备战中考寒假系列答案
备战中考寒假系列答案【题目】小强同学前往当地的石灰石矿区进行调查,他取回了若干块矿石样品,对样品中碳酸钙的质量分数进行检测,采用的办法如下:取用8 g这种石灰石样品,把40 g稀盐酸分4次加入,测量过程所得数据见下表(已知石灰石样品中含的杂质不溶于水,不与盐酸反应)。请计算:
(1)8 g石灰石样品中含有杂质多少克____________?
(2)样品中碳酸钙的质量分数是多少_________________?
(3)下表中m的数值应该为多少____________?
序号 | 加入稀盐酸质量/g | 剩余固体质量/g |
第1次 | 10 | 5.5 |
第2次 | 10 | m |
第3次 | 10 | 1.2 |
第4次 | 10 | 1.2 |
(4)要得到280 kg CaO,需要质量分数为80%的石灰石多少千克_____________?(化学方程式:CaCO3![]() CaO+CO2↑)
CaO+CO2↑)
【题目】化学教材“寻找新的催化剂”研究性实验,引起了化学探究小组的兴趣.
(提出问题)(1)氧化铁(Fe2O3)能否作过氧化氢溶液分解的催化剂?
(2)氧化铁与二氧化锰催化效果哪个好?
(3)催化剂的质量是否对过氧化氢溶液分解的速率产生影响?
(实验探究)
实验步骤 | 实验现象 |
①分别量取5mL15%过氧化氢溶液放入A、B两支试管中,向A试管中加入ag氧化铁粉末,并分别在A、B两支试管中插入带火星的木条,观察现象 | A试管中产生大量气泡,带火星木条复燃, B试管中的现象:…… |
②待A试管中没有现象发生时,重新加入过氧化氢溶液,并把带火星的木条伸入试管内,如此反复多次实验,观察现象 | 试管中均产生大量气泡,带火星木条均复燃 |
③将实验②中的剩余物小心过滤,并将所得滤渣进行洗涤、干燥、称量,所得固体质量仍为ag | |
④分别量取5mL15%过氧化氢溶液放入C、D两支试管中,向C试管中加入ag氧化铁粉末,向D试管中加入ag二氧化锰粉末,观察现象 |
(1)A试管中反应的符号表达式为_________;B试管中的现象________。
(2)实验②、③证明:氧化铁的___________和____在反应前后均没有发生变化,可以作过氧化氢分解的催化剂;
(3)实验设计④的目的是_________,若实验![]() 观察到D试管中产生气泡的速率更快,由此你可以得到的结论是____。
观察到D试管中产生气泡的速率更快,由此你可以得到的结论是____。
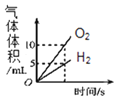
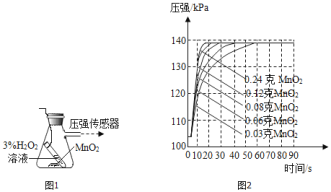
(4)兴趣小组同学设计了如图1实验装置,利用压强传感器测不同质量二氧化锰对双氧水分解快慢的影响。在8mL3%的双氧水中分别加入了0.03g,0.06g,0.08g,0.12g,0.24gMnO2测得容器内压强的变化曲线如图2所示![]() 曲线的斜率表征催化反应的速率
曲线的斜率表征催化反应的速率![]() 请观察如图,回答问题:
请观察如图,回答问题:
![]() Ⅰ
Ⅰ![]() 根据图2可发现:该实验条件下,30s内催化分解8mL浓度为
根据图2可发现:该实验条件下,30s内催化分解8mL浓度为![]() 的双氧水,MnO2的最小用量为_____g。
的双氧水,MnO2的最小用量为_____g。
![]() Ⅱ
Ⅱ![]() 根据图2,下列说法正确的是________。
根据图2,下列说法正确的是________。
a 二氧化锰用量越多,产生氧气越多
b 反应容器的气密性,对实验所测数据的精确度有影响
c 称量的二氧化锰质量的精确度对实验装置中最终的压强大小没有影响
(知识拓展)
若实验中ag氧化铁中a=0.25,则其中氧元素的质量为__________g。若经过精密仪器测得该氧化铁样品中铁元素和氧元素的质量比为21∶8,则该氧化铁样品中混有的另一物质是___________(填“FeO”或“Fe3O4”)
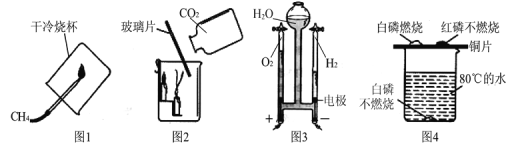
【题目】化学是一门以实验为基础的科学,几位同学对化学实验非常感兴趣,请结合图表信息回答问题:
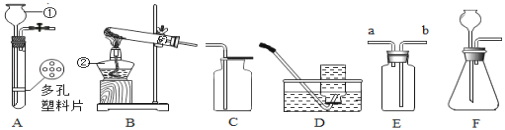
Ⅰ写出图中①②仪器的名称:①_____,②_____。
Ⅱ甲同学在实验室用加热高锰酸钾的方法制取氧气,反应的化学方程式为_____,发生装置是_____,加热时试管口应略向下倾斜的原因是_____。
Ⅲ乙同学在实验室研究二氧化碳的制备和性质。
制备二氧化碳的化学方程式是_____;他选用了A而没有选用F做发生装置,是因为A的优点是_____;他用E装置收集该气体,气体应从_____(填“a”或“b”)端通入;他在收集得到二氧化碳的集气瓶中滴加适量澄清石灰水,稍作振荡,发生的现象是_____,反应的化学方程式是_____。
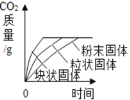
IV丙同学研究实验室制取二氧化碳的适宜条件(温度、酸的浓度、大理石固体的颗粒大小等因素会影响化学反应的快慢),进行了如下四组实验:
实验编号 | A | B | C | D |
mg大理石 | 块状 | 块状 | 粉末状 | 粉末状 |
ng盐酸(过量) | 稀盐酸 | 浓盐酸 | 稀盐酸 | 浓盐酸 |
实验A与_____对照(填编号),是为了研究固体反应物颗粒大小对反应快慢的影响;上述实验中,另一个影响反应快慢的因素是_____。
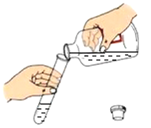
V丁同学研究了木条复燃与氧气体积分数的关系,发现不纯的氧气也能使带火星的木条复燃。他想收集一瓶混有约1/4体积空气的氧气,应该选用_____(填序号)完成实验,收集好后集气瓶中氧气的体积分数约为_____(空气中氧气的含量按照1/5计算)。
A 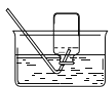 集气瓶中灌1/4的水 B
集气瓶中灌1/4的水 B 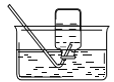 集气瓶中灌3/4的水
集气瓶中灌3/4的水
C ![]() 导管伸入到集气瓶体积的1/4处 D
导管伸入到集气瓶体积的1/4处 D ![]() 导管伸入到集气瓶体积的3/4处
导管伸入到集气瓶体积的3/4处
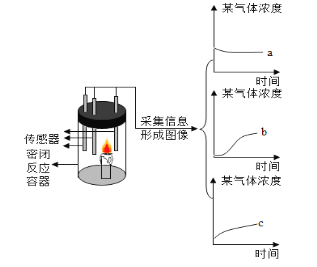
VI戊同学利用数字化实验探究蜡烛的燃烧,如图所示,蜡烛在密闭容器内燃烧,同时监测容器内氧气、二氧化碳和水蒸气含量的变化,形成三条曲线如下坐标图所示a、b、c。曲线_____(填“a”“b”或“c”)能够说明蜡烛燃烧消耗氧气。