题目内容
【题目】实验室中,利用下列装置可以制取某些气体,请回答下列问题。
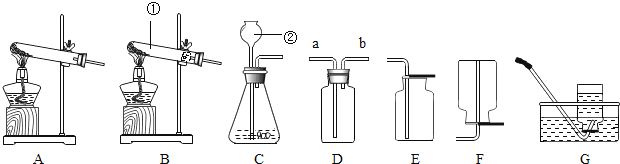
(1)写出装置中标号仪器的名称:①______
(2)实验室用高锰酸钾制取氧气时.应选用的发生装置是______(填字母),反应的化学方程式为______
(3)如果用D装置收集氧气,则氧气由______端通入(填“a”或“b” )
(4)若用B、G装置制取氧气,将收集满气体的集气瓶取出水槽正放在桌子上,接下来的操作是先______
【答案】试管 B ![]() a 先将导管从水槽中移出,再熄灭酒精灯
a 先将导管从水槽中移出,再熄灭酒精灯
【解析】
(1)从图中可知①是试管;
(2)高锰酸钾加热生成锰酸钾、二氧化锰和氧气,高锰酸钾是固体需要加热;
(3)氧气的密度比空气密度大,应用向上排空气法收集,所以从a进;
(4)高锰酸钾制取氧气并用排水法收集氧气时要先将导管从水槽中移出,再熄灭酒精灯以防止水倒吸炸裂试管;

 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案【题目】做完“铁丝在氧气中燃烧”实验后,小冬同学有两个疑惑不解的问题,于是他进行了以下探究活动,请你一同参与。
(问题1)铁丝燃烧时溅落下来的黑色高温熔化物中还有没有铁呢?
(查阅资料1)(1)自然界中铁的氧化物主要是![]() 和
和![]() 两种(
两种(![]() 极易被氧化为
极易被氧化为![]() );
);
(2)铁的氧化物均能溶于酸的溶液。
(实验探究)将冷却后的黑色物质碾碎,装入试管,加入______溶液,观察到的现象是______,说明铁燃烧时溅落下来的黑色物质中还有含有铁。
(问题2)铁燃烧的产物为什么不是![]() 呢?
呢?
(查阅资料2)
(1)![]() 和
和![]() 的分解温度、铁的熔点见右表:
的分解温度、铁的熔点见右表:
|
|
| |
分解温度 | 1538℃ | 1400℃ | — |
熔点 | — | — | 1535℃ |
(2)![]() 高温时分解成
高温时分解成![]()
(理论探讨)
根据实验现象,并结合表中数据,可推知铁丝在氧气中燃烧时所产生的高温应该在______之间,在此温度范围内![]() 已分解,所以铁在氧气中燃烧产生的是
已分解,所以铁在氧气中燃烧产生的是![]() 。
。
A.1400℃~1535℃ B.1400℃~1538℃ C.1535℃~1538℃
(拓展延伸)
(1)请写出铁丝在氧气中燃烧的化学方程式:______。
(2)实验中为了防止集气瓶炸裂,必须______。
(3)有些超市的食品密封包装盒的透明盖内放有黑色的![]() 粉末,若粉末的颜色______
粉末,若粉末的颜色______
【题目】某反应的微观示意图如下,有关该反应的说法,不正确的是( )
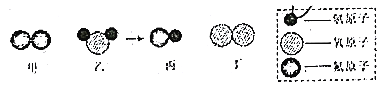
A. 该反应属于置换反应
B. 参加反应的甲和乙的分子个数比为1:1
C. 其中有两种物质属于氧化物
D. 该反应中甲与丁的质量比为19:8
【题目】常温下没有氧气存在时,铁与水几乎不反应,但高温下,铁与水蒸气能反应生成一种常见铁的氧化物和一种气体。小明很好奇,设计如下实验探究铁粉与水蒸气反应后的产物。
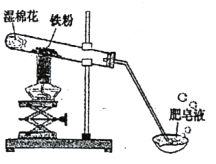
(1)试管尾部放一团湿棉花的作用是____________。
(2)探究生成的气体是什么?用燃着的木条靠近肥皂泡,有爆鸣声,稍后有肥皂泡飘到空中。说明生成的气体是_________________。
(3)探究试管中剩余固体成分是什么?
(查阅资料)
常见铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
颜色、状态 | 黑色粉末 | 红棕色粉末 | 黑色晶体 |
能否被磁铁吸引 | 否 | 否 | 能 |
金属氧化物可以与酸反应,生成水和另一种金属化合物(如:CuO+2HCl=CuCl2+H20)。
(初步验证)试管中剩余固体为黑色,能全部被磁铁吸引。
(猜想与假设)猜想一:剩余固体是Fe与Fe3O4;
猜想二:剩余固体是__________。
(实验探究)
实验操作 | 实验现象 | 结论 |
取少量黑色固体于试管中,加入足量的稀盐酸。 | ________________ | 猜想一正确 |
________________ | 猜想二正确 |
(实验结论)铁和水蒸气反应的化学方程式为_____________。
(反思与交流)该黑色固体不可能是Fe2O3,理由是_____________。