题目内容
【题目】鸡蛋壳的主要成分是碳酸钙,为了测定某鸡蛋壳中碳酸钙的含量,小群同学进行了如下实验:将鸡蛋壳洗净、干燥并捣碎后,称取10g放在烧杯里,然后往烧杯中加入足量的稀盐酸90g,充分反应后,称得烧杯中物质的总质量为97.8g。(假设鸡蛋壳中的其他物质不与盐酸反应)
(1)产生二氧化碳气体______g。
(2)10g该鸡蛋壳中最酸钙首质量是____g,要求写出完整的解题步骤。
【答案】2.2g 5g
【解析】
(1)鸡蛋壳中只有碳酸钙和盐酸反应生成二氧化碳气体,反应前物质的总质量=10g+90g=100g,反应后物质的总质量还剩97.8g,根据质量守恒定律,产生二氧化碳的质量=100g﹣97.8g=2.2g故填2.2;
(2)根据化学方程式进行计算,完整步骤为:
解:设10g该鸡蛋壳中碳酸钙的质量为x,
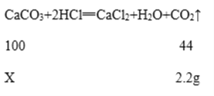
![]() =
=![]()
解得X=5g,
答:10g该鸡蛋壳中碳酸钙的质量为5g。
计算10g该鸡蛋壳中碳酸钙的质量故填5g。

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目