题目内容
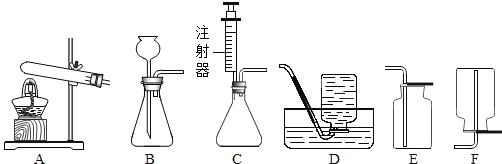
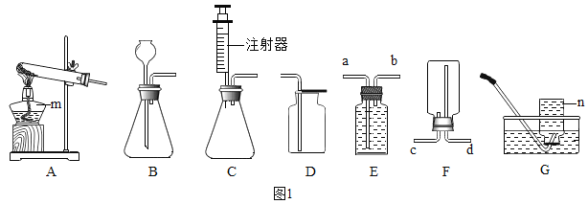
【题目】实验室中,利用下列装置可以制取某些气体,请回答下列问题。
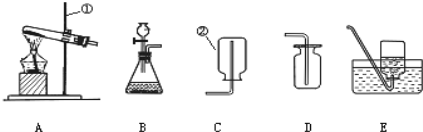
(1)写出上述标号仪器的名称①______; ②__________;
(2)向气体发生装置内加入药品前,应该进行的操作是_________;
(3)林月用高锰酸钾制取氧气,她选择上述装置中的A作为发生装置,你认为A装置中还缺少_________
(4)若实验时用过氧化氢代替高锰酸钾加热制氧气,优点是______(填序号)
A.生成物中只有氧气B.不需加热C.需加热
(5)实验室若用双氧水制取氧气,选择的发生装置是__________;收集氧气可选择的装置是_________
(6)小阳同学用加热醋酸钠和碱石灰(均为固体)的方法制取甲烷。甲烷是一种无色无味,难溶于水,密度比空气小的气体。小阳应选择的发生装置是___,收集装置是_____。(填字母)
【答案】铁架台 集气瓶 检查装置的气密性; 棉花; B B; D(或E) A C(或E)
【解析】
(1)仪器①的名称为铁架台;仪器②的名称为集气瓶;
(2)向气体发生装置内加入药品前,应该进行的操作是检查装置的气密性;
(3)高锰酸钾制取氧气应在试管口放一团棉花,防止高锰酸钾进入导管引起堵塞;
(4)A、过氧化氢分解生成氧气和水,选项错误;B、该反应无需加热即可分解出氧气,选项正确;C、由B分析可知,选项错误。故本题选B;
(5)实验室若用双氧水制取氧气,反应无需加热,故选择的发生装置是B;氧气密度大于空气,且氧气不易溶于水,故可用排水法或者向上排空气法进行收集,故收集装置选D或者E;
(6)醋酸钠和碱石灰(均为固体)的方法制取甲烷需要进行加热,故发生装置选A;甲烷难溶于水,密度比空气小,故可采用排水法或者向下排空气法进行收集,故收集装置选C或者E。

【题目】小芳发现,氯酸钾与氧化铜混合加热,也能较快产生氧气,于是进行如下探究:
(提出猜想)除二氧化锰、氧化铜外,氧化铁也可以作氯酸钾分解的催化剂。
(完成实验)按下表进行实验:测定分解温度(分解温度越低,催化效果越好)。
实验编号 | 实验药品 | 分解温度 |
① | 氯酸钾 | 580℃ |
② | 氯酸钾、二氧化锰(质量比 1:1) | 350℃ |
③ | 氯酸钾、氧化铜(质量比 l:1) | 370℃ |
④ | 氯酸钾、氧化铁(质量比 1:1) | 390℃ |
(分析数据、得出结论)
(1)由实验_____对比,证明猜想合理;
(2)实验所用的三种金属氧化物,催化效果最好的是_____。
(3)若氧化铁是该反应的催化剂,请写出这个反应的文字表达式_____。
(4)如表是二氧化锰用量与一定质量氯酸钾制取氧气反应速率关系的实验数据。
①据如表可知二氧化锰与氯酸钾的质量比为_____时,反应速率最快;
②通过分析可知,在化学反应中催化剂的用量_____越多越好。(填“是”或“不是”)
③二氧化锰用量过多冲淡了氯酸钾粉末,相当于减少反应物的_____,所以反应速率受到影响。