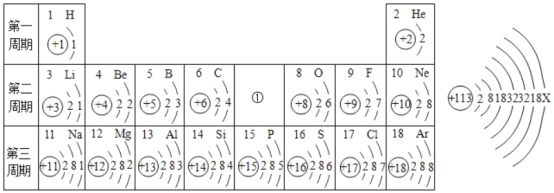
题目内容
【题目】小关键同学在实验室探究金属的某些物理性质和化学性质,部分操作如图所示。
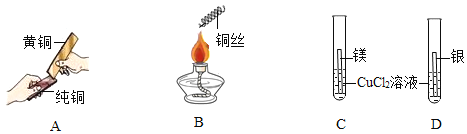
(1)操作A中能说明黄铜的硬度比纯铜大的现象为______。
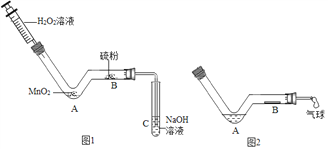
(2)操作B中可观察到的现象为______。
(3)操作C、D可以判断金属镁、银、铜的金属活动性顺序,操作C中发生反应的化学方程式为____。
(4)如果只用三种试剂,验证铝、铁、铜的金属活动性强弱,可选择的三种试剂为______。
(5)室温下,将锌片和铁片( 用M或N标识) 分别与稀盐酸反应,产生氢气。图象如图:
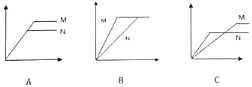
①将等量的锌片、铁片分别与足量的稀盐酸反应,产生氢气的质量与时间的关系图序为______。(填字母序号,下同)
②将足量的锌片、铁片分别与等量的稀盐酸反应,产生氢气的质量与时间的关系图序为______。
③将足量的锌片、铁片分别缓慢加入等量的稀盐酸中,产生氢气的质量与加入金属的质量的关系图序为______。
④将足量的稀盐酸分别缓慢加入等量的锌片、铁片中,产生氢气的质量与加入盐酸的质量的关系图序为______。
【答案】纯铜表面留下划痕 铜丝表面变黑 Mg+CuCl2=MgCl2+Cu 铝、铜和硫酸亚铁溶液或硫酸铝溶液、铁、硫酸铜溶液 C B B A
【解析】
(1)操作A中能说明黄铜的硬度比纯铜大的现象为纯铜表面留下划痕。
(2)操作B中,铜和氧气反应生成黑色氧化铜,可观察到的现象为铜丝表面变黑;
(3)操作C中镁和氯化铜反应生成氯化镁和铜,发生反应的化学方程式为:Mg+CuCl2=MgCl2+Cu。
(4)在验证三种金属的活动性时常用三取中的实验方法,可以取金属活动顺序表中位于两边的金属和中间金属的盐溶液,因为金属活动性铝>铁>铜,所以可选择的三种试剂为铝、铜和硫酸亚铁溶液;
(5)①将等量的锌片、铁片分别与足量的稀盐酸反应,由于锌的活动性大于铁,锌反应的要剧烈,完全反应后相同质量的锌、铁,铁生成氢气的质量多,所以产生氢气的质量与时间的关系图序为C;
②将足量的锌片、铁片分别与等量的稀盐酸反应,由于锌的活动性大于铁,锌反应的要剧烈;由于稀盐酸少量但相等,故完全反应后生成氢气的质量一样多,所以产生氢气的质量与时间的关系图序为B。
③将足量的锌片、铁片分别缓慢加入等量的稀盐酸中,等质量的金属铁生成的氢气质量多,完全反应后产生氢气的相同,反应产生氢气的质量与加入金属的质量的关系图序为B。
④将足量的稀盐酸分别缓慢加入等量的锌片、铁片中,等质量的酸反应生成的氢气质量相同,等质量的金属完全反应铁生成的氢气多,产生氢气的质量与加入盐酸的质量的关系图序为A。