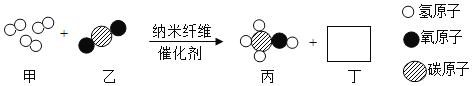
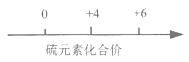
题目内容
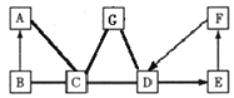
【题目】核电荷数为1~18的元素的原子结构示意图等信息如下,请回答下列间题
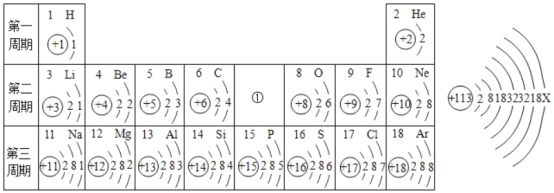
(1)写出位于周期表中所标①处的化学符号_____
(2)下列各组具有相似化学性质的元素是_____(填字母序号);
A Na、Cl B O、Si C F、C1 D He、Mg
(3)笫17号元素与笫12号元素的原子形成化合物的化学式为_____;
(4)2017年5月9日,我国发布了新发现的四种元素的中文名称。其中113号元素的元素符号为Nh,中文名称为“鉨”。如图为鉨原子结构示意图,x=_____,该元素位于第_____ 周期,鉨原子形成离子的符号为_____。
【答案】N; BC; MgCl2; 3; 7; Nh3+。
【解析】
(1)同一周期,从左到右,原子序数依次增大,位于周期表中所标①处的化学符号N;
(2)最外层电子数相同,化学性质相似,
A、Na、Cl 的 最外层电子数不相同,化学性质不相似;
B、O和S的最外层电子数都为6,化学性质相似;
C、F、C1的最外层电子数都为6,化学性质相似;
D、He属于稳定结构,与Mg的化学性质不相似;
(3)17号是氯元素,常显﹣1价,12号是镁元素,常显+2价,二者组成的化合物是氯化镁,其化学式为MgCl2;
(4)在原子中质子数等于电子数,所以甲中x=113﹣2﹣8﹣18﹣32﹣32﹣18=3。
电子层数决定周期数,该元素位于第7周期,
由于鉨元素原子的最外层电子数是3,小于4,在化学反应中易失去,鉨原子形成离子的符号为:Nh3+。

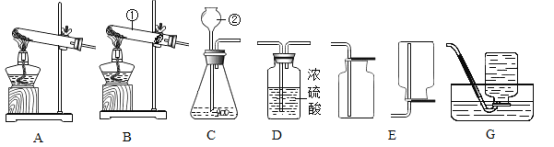
【题目】兴趣小组同学发现实验台上整齐摆放的药品中(见图),有一试剂瓶的标签破损。
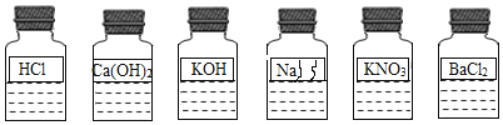
(讨论)根据受损标签及实验室药品分类摆放的原则,这瓶试剂不可能是_____(填序号)。
A 酸 B 碱 C 盐
(提出问题)这瓶试剂的成分是什么?
(猜想)实验老师告诉同学们该瓶试剂有段时间曾忘记盖试剂瓶盖。可能是以下三种情况中的一种
①NaOH溶液;②可能是Na2CO3溶液;③可能是NaCl溶液
(查阅资料)KNO3和BaCl2溶液都呈中性
(设计并实验)
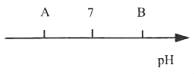
(1)甲同学用洁净干燥的玻璃棒蘸取该溶液滴到湿润的pH试纸上,测得pH=10,他判断这是一种碱性溶液,从而排除第③种可能。对他的操作方法、测量结果及结论的评价,正确的是_____(填序号)。
A 方法正确,结果正确,且结论正确 B 方法不正确,结果偏小,但结论正确
C 方法不正确,结果偏大,结论不正确 D 方法正确,结果正确,但结论不正确
(2)要进一步确定它的成分,老师提示只需选择上图已有的试剂和酸碱指示剂就能把它鉴别出来。乙丙丁三位同学他们又进行了实验。
实验操作 | 实验现象 | 实验结论 | |
乙同学 | 取少量试剂于试管中,加入足量的Ca(OH)2溶液。过滤,向滤液中滴入无色酚酞 溶液 | _____ | 认为是氢氧化钠且部分变质 |
丙同学 | 取少量试剂于试管中,加入适量_____的溶液。 | 有气泡产生 | 认为是碳酸钠 |
(评价反思)
你认为乙和丙两位同学的设计方案和结论_____(正确或不正确)
(总结提高)请你选择上图已有的试剂和常见的酸碱指示剂完成你的设计。
实验操作 | 实验现象 | 实验结论 |
取少量试剂于试管中,加入足量_____溶液,过滤,向滤液中滴入无色酚酞溶液 | _____ | 是氢氧化钠且部分变质 |