题目内容
【题目】某同学在实验室发现一瓶由碳酸钠和氯化钠组成的混合溶液。为了测定此混合溶液中碳酸钠的质量分数,该同学设计如下实验:取此混合溶液53g,向其中滴加稀盐酸,当加入稀盐酸的质量为10g、20g、30g、40g时,生成气体的质量见下表(气体的溶解度忽略不计)。
第I组 | 第Π组 | 第Ⅲ组 | 第Ⅳ组 | |
稀盐酸的质量/g | 10 | 20 | 30 | 40 |
生成气体的质量/g | 0.9 | m | 2.2 | 2.2 |
请计算:
(1)第Π组数据m为_________;
(2)混合溶液中碳酸钠的质量分数是多少_____?
【答案】1.8g 10%。
【解析】
(1)由于第一次加入盐酸生成气体是0.9g,而第三次相对假如第二次加入时每次加入10g盐酸都对应0.9g还是有气体生成的,所以可以确定第二次也是每10g盐酸生成0.9g气体,即m为1.8g;
(2)由表中信息可知25g该混合溶液中碳酸钠与稀盐酸充分反应生成2.2g二氧化碳气体
设:该混合溶液中碳酸钠的质量为x,
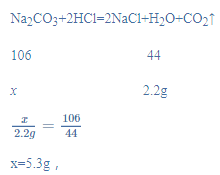
该混合溶液中碳酸钠的质量分数=![]() ×100%=21.2%;
×100%=21.2%;
答:混合溶液中碳酸钠的质量分数为21.2%。

练习册系列答案
相关题目