��Ŀ����
����Ŀ���Ķ�������ն��ġ�
���й��Ŵ�������չ����ʷ�����У��ҹ��Ŵ��������ڻ�ҩ�������մɡ���ͭұ���Ȼ�ѧ�ӹ���������ȡ��������Ƿ��ijɾͣ�Ϊ�ٽ��ҹ��Ŵ���ᷢչ������Ľ����������ش�Ĺ��ס�
����ҩ����������ʹ�õĻ�ҩ�Ǻڻ�ҩ����Ҫ��Ӧ���£�

�������մɡ������������������ڹ�����ϵ����Ʒ������Ҫ�Ļ�ѧ�ɷ��Ƕ������裨SiO2������������Al2O3�������ֽ�����Ca��Mg��Fe��K��Na�ȣ���������ڻ�ѧ�ɷֺ�������;�ȷ���ȴ��������
��Ʒ | ��ѧ�ɷ� | ������;�� |
���� | Al2O3 Լ15%��18%�� Fe2O3Լ5%��6%�� CaO��MgO�ȡ�3%�� | �ֲڣ�������Ӳ��������ȡˮ��ʢ��ʳ��ȡ� |
���� | Al2O3 Լ18%��28%�� Fe2O3Լ1%��2%�� CaO��MgO�ȡ�1%�� | �����սᣬ��Ӳ���ܣ���ף����� �ʰ������û�ʱ����ö������ۣ���;�㷺�����͡��ղؼ�ֵ�ߵȡ� |
������ұ�������շ�չ�����ĸ��¼���Ϊ������ұ���������������������ҹ�����ʯ��ʱ������������������ͭ����Ϊ����ͭ��ʱ������������������Ϊ������ʱ�������Ľ���ʱ����
��ͭұ��
��Ȼͭ������ͭ��ʯ֮�У������ڼ����ۻ���Ȼͭ�Ĺ����У�����ɫ�Ŀ�ȸʯ[Cu2(OH)2CO3]���ػ��ɫ����ʯ��SnO2������ɫ�ķ�Ǧ��PbS������һ���գ����������ͭ����ͭ��ͭ������Ǧ�۳ɵĺϽ��۵�ȴ�ͭ��1083�棩��100�桫300�棬���ӹ������죬��������Ҳ�ȴ�ͭ�ã�Ӳ�ȼ������һ�����ʺ��������ߺͱ�����
����ұ��
���˴����к��ڣ��ҹ�����������Ϥ�������˿������������������������ȷ������Ը���Һ�廹ԭ��ұ�������ļ���������ұ��ʷ����һ����ʱ���Ľ�����
�������������Ľ���������Ҳ���������֡������ֶ�����̼�Ͻ𡣺�̼��>2%��Ϊ��������̼��<0.02%��Ϊ��������̼��������֮��Ϊ�֡������������ݻش��������⡣
��1���ڻ�ҩ����Ҫ�ɷ���________��
��2�������������ѧ�ɷֵ���Ҫ������_________��
��3��������̼����______������ڡ����ڡ����ֵ�̼������
��4���봿������ȣ��Ͻ���ŵ������________��
���𰸡� ����ء�ľ̿����KNO3 ��C��S�� �մ���Al2O3�����ȴ����ͣ�Fe2O3��CaO��MgO�����ȴ����� ���� Ӳ�ȴ��۵��
�����������⿼���˸��ݶ��ĺڻ�ҩ�������������ѧ�ɷ֣����Ͻ�ijɷֺ����ʣ������Ķ������ǽ���Ĺؼ���
��1���������ṩ�Ļ�ѧ����ʽ��֪���ڻ�ҩ����Ҫ�ɷ�������ء�ľ̿����KNO3 ��C��S����
��2�����������������ѧ�ɷֱ���֪�������������ѧ�ɷֵ���Ҫ���������մ���Al2O3�����ȴ����ͣ�Fe2O3��CaO��MgO�����ȴ����ߣ�
��3�������ֶ�����̼�Ͻ𡣺�̼��>2%��Ϊ��������̼��<0.02%��Ϊ��������̼��������֮��Ϊ�֡�������̼�������ڸֵ�̼������
��4���봿������ȣ��Ͻ���ŵ��������Ӳ�ȴ��۵�͡�
�����͡�������
��������
21
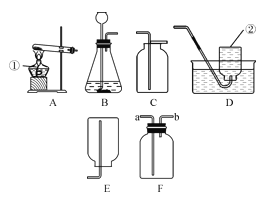
����Ŀ����ҵ����ȡ�����(NH4NO3)������ͼ���£���ش��������⡣
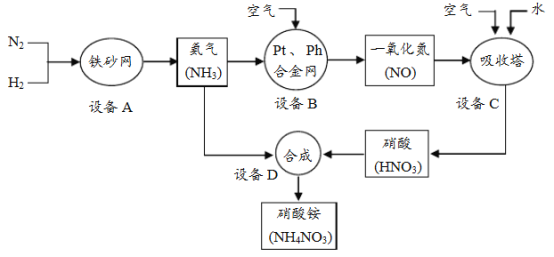
��1���豸A�У������ķ�Ӧ���ڻ�����Ӧ�����е�________��
��2���豸B��C�У������е�______һ���μ��˷�Ӧ��
��3���豸C�У�������������ų��ķ����лẬ��һЩ���������������������
����������
����һ��NaOH��Һ���շ���NO + NO2 + 2NaOH �� 2NaNO2 + H2O
��������NH3��ԭ����8NH3 + 6NO2![]() 7N2 + 12H2O��NOҲ�����Ƶķ�Ӧ��
7N2 + 12H2O��NOҲ�����Ƶķ�Ӧ��
�������ַ����У�����Ϊ���ַ����ò�˵������________��
��4���豸D�У���NH3��HNO3�Ʊ�NH4NO3��NH4NO3�е�Ԫ�����������ļ���ʽΪ________��
���𰸡� ���Ϸ�Ӧ ���� ����һ�������У������������� ![]()
�������������ù�ҵ����ȡ�����(NH4NO3)������ͼ�������Ķ������Ϣ���������ڣ�2�����и��������غ���з�����
��1���豸A�У�������N2��H2������NH3�ķ�Ӧ�����ڻ�����Ӧ�����еĻ��Ϸ�Ӧ��
��2���豸B�� NH3��NO���豸C��NO��HNO3�����������غ㶨�ɣ����豸B��C�У������е�����һ���μ��˷�Ӧ��
��3������һ�ڳ��¾��ܷ�����ѧ��Ӧ������һ�������У���������NH3 �� NO��Ӧ���˵�����ˮ������Ⱦ����������������
��4��NH4NO3�е�Ԫ����������=![]()