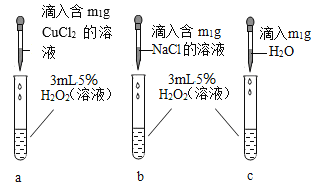
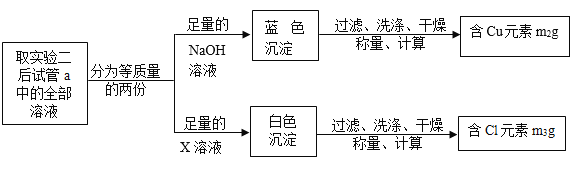
题目内容
【题目】经过学习,你一定掌握了相关气体的制备方法。现有下列实验装置图,回答问题:
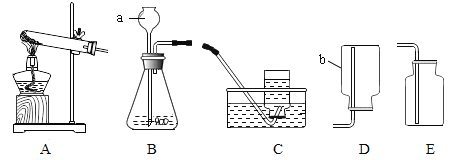
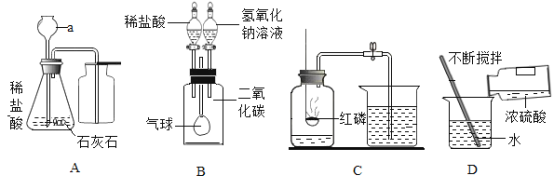
(1)仪器a的名称是____;
(2)用A与C相连可制取一种气体,写出该反应的化学方程式为________;
(3)氨气是一种密度比空气小,极易溶于水的气体,则收集氨气应选择____装置。
【答案】长颈漏斗 2KClO3![]() 2KCl+3O2↑ D
2KCl+3O2↑ D
【解析】
(1)仪器a是长颈漏斗;故填:长颈漏斗;
(2)A装置与C装置连接可制取由固体和固体反应,需要加热,生成的气体不溶于水且不与水反应,适合实验室用氯酸钾和二氧化锰制取氧气,氯酸钾在二氧化锰催化作用下分解生成氯化钾和氧气,反应的方程式为:2KClO3![]() 2KCl+3O2↑;故填:2KClO3
2KCl+3O2↑;故填:2KClO3![]() 2KCl+3O2↑;
2KCl+3O2↑;
(3)氨气是一种密度比空气小,且极易溶于水的气体,因此只能用向下排空气法收集。故填:D。

 计算高手系列答案
计算高手系列答案【题目】请从A或B两题中任选一个作答,若两题均作答,按A计分。
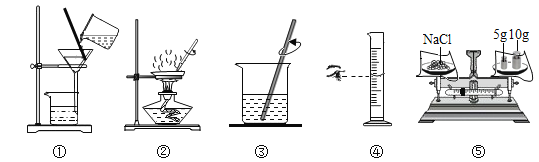
A去除粗盐中的泥沙 | B配制160g10%的氯化钠溶液 |
(1)实验的主要步骤是: ③→_____→_____(填序号,下同)。 (2)蒸发时,用玻璃棒搅拌的目的是 _____。 | (1)实验的主要步骤是: ⑤→_____→_____。 (2)溶解时,用玻璃棒搅拌的目的是 _____。 |
可供选择的基本实验操作如下图:
| |
【题目】结合下列装置回答问题。
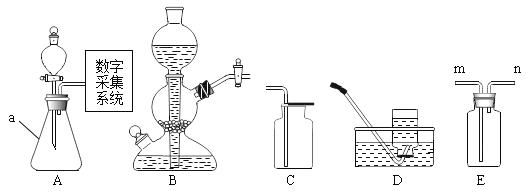
①仪器a的名称是_________________。
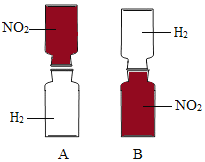
②装置B中的活塞处于______ (选填“开启”或“关闭”)状态。
③实验室制取二氧化碳的化学方程式为______, 若用装置E收集二氧化碳,验满时燃着的木条应放在______(选填“m”或“n”)端。
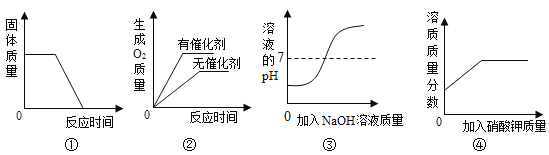
④化学兴趣社团借助数学化实验手段用装置A探究“外界条件对过氧化氢分解速率的影响”,按下表分组进行实验一, 在同一温度下通过压强传感器得到的数据如下图所示。

实验一 | 药品 |
第一组 | 4%H2O2溶液15mL |
第二组 | 4%H2O2溶液15mL、0.2gMnO2粉末 |
第三组 | 4%H2O2溶液15mL、0.2gFeCl3粉末 |
I .经过分组实验,同学们从实验一中得出结论: 在其他条件相同的情况下,____ (填物质名称)作催化剂的催化效果最好。
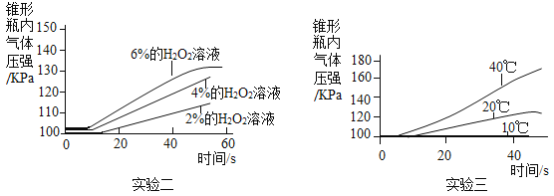
II .选用0.2g的MnO2粉末做催化剂,同学们又分别做了实验二和实验三,得到的数据图表如上,你认为影响该反应速率的外界因素除催化剂外,还有_________。
Ⅲ.实验一与实验二中4%的过氧化氢溶液与0.2g MnO2粉末混合后产生的气体压强有明显不同(见图中A点和B点),你认为可能的原因是_________。
⑤小组同学若利用过氧化氢制取0.1mol氧气,需要过氧化氢的物质的量为多少_____?(根据化学方程式计算)