题目内容
【题目】学习了金属的有关知识后,同学们知道了如何鉴别黄金和黄铜(铜锌合金,俗名“愚人金”)。某化学兴趣小组的同学为了进一步测定某黄铜的组成,称取了黄铜样品50g放入锥形瓶中,向其中分5次共加入250g稀硫酸,测得数据记录如下表。
次数 质量 | 第1次 | 第2次 | 第3次 | 第4次 | 第5次 |
累计加入稀硫酸的质量/g | 50 | 100 | 150 | 200 | 250 |
累计产生气体的质量/g | 0.2 | x | 0.6 | 0.7 | 0.7 |
回答下列问题:
(1)x=__,该样品中铜的质量为__g。
(2)请在如图中画出样品中加入250g稀硫酸,产生气体的质量与稀硫酸的质量变化关系示意图。

(3)黄铜样品与稀硫酸恰好完全反应时,所得溶液的溶质的质量分数是_____?(精确到0.01)
【答案】0.4、27.25g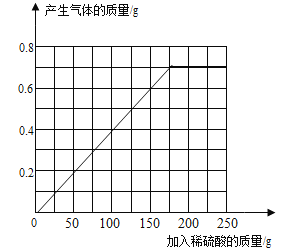 28.61%
28.61%
【解析】
根据第一次和第三次可以看出,每25g硫酸对应0.1g氢气,所以可以确定x=0.4,而生成0.7g氢气也就是加入175g稀硫酸时恰好完全反应,据此分析和解答。
解:(1)根据第一次和第三次可以看出,每25g硫酸对应0.1g氢气,所以可以确定x=0.4,而生成0.7g氢气也就是加入175g稀硫酸时恰好完全反应;设恰好完全反应时生成的硫酸锌的质量为x,反应的锌的质量为y,
Zn+H2SO4=ZnSO4+H2↑
65 161 2
y x 0.7g
![]() x=56.37g,
x=56.37g,
![]() y=22.75g,
y=22.75g,
所以该样品中铜的质量为:50g-22.75g=27.25g;
(2)根据第一次和第三次可以看出,每25g硫酸对应0.1g氢气,生成0.7g氢气也就是加入175g稀硫酸时恰好完全反应,产生气体的质量与稀硫酸的质量变化关系示意图为:
(3)黄铜样品与稀硫酸恰好完全反应时,所得溶液的溶质的质量分数为:![]() =28.61%;
=28.61%;
答:(1)x=0.4,该样品中铜的质量为27.25g;(2)样品中加入250g稀硫酸,产生气体的质量与稀硫酸的质量变化关系示意图: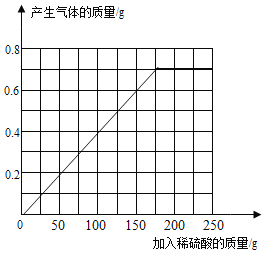
(3)黄铜样品与稀硫酸恰好完全反应时,所得溶液的溶质的质量分数是28.61%。