题目内容
(6分)把6.5g 锌放入到50g 硫酸溶液恰好完全反应。计算:
可制得氢气多少克?
这种硫酸溶液中溶质的质量分数是多少?
可制得氢气多少克?
这种硫酸溶液中溶质的质量分数是多少?
①0.2g②19. %
试题分析:(1)根据题意可知:已知量为锌的质量;未知量为氢气的质量和硫酸溶液的溶质质量分数。解题思路:可根据锌与硫酸、氢气在反应过程中的质量关系进行求解。具体过程如下:
解:设可制得氢气的质量为x,得到硫酸锌的质量为y
Zn + H2SO4 ="===" ZnSO4+ H2↑
65 98 2
6.5g y x
65:2=6.5g:x
x=0.2g
65:98=6.5g:y
y=9.8g
(2)这种硫酸溶液中溶质的质量分数:
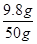 ×100%=19.6%
×100%=19.6%答:①可制得氢气0.2g;②硫酸溶液中溶质的质量分数是19.6%

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目


