题目内容
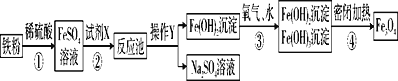
【题目】海洋中有丰富的水生生物和化学资源,海带就是其中之一。从海带中提取碘的流程如下:
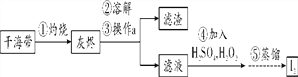
(1)写出④中氧化物的名称______________________。
(2)第①步中将“干海带灼烧”的目的是_____________。
(3)操作a的名称是________________,该操作中玻璃棒的作用是_______________
(4)海带灰烬中含有碳酸钾,为了使溶液呈弱酸性,加入硫酸酸化,发生反应的化学方程式为 ______________。
(5)判断提取物是否含有碘的方法是________________
【答案】 过氧化氢 除去海带中的有机物,有利于溶解 过滤 引流 K2CO3+H2SO4= K2SO4+H2O+CO2↑ 取少量的溶液,向溶液中加入淀粉溶液,若溶液呈蓝色,则有碘存在
【解析】(1)根据物质的组成分析解答;
(2)根据燃烧能使海带中的有机物充分反应分析解答;
(3)根据分离固液混合物解答;
(4)硫酸和碳酸钾充分反应生成硫酸钾、水和二氧化碳;
(5)根据碘的检验方法解答。
解:(1)氧化物由两种元素组成,其中一种元素是氧元素的化合物。由此可知,④中氧化物是H2O2,其名称为:过氧化氢;
(2)第①步中将“干海带灼烧”的目的是:除去海带中的有机物,有利于溶解;
(3)操作a的名称是过滤;该操作中玻璃棒的作用是引流;
(4)硫酸和碳酸钾充分反应生成硫酸钾、水和二氧化碳,反应的化学方程式为:K2CO3+H2SO4= K2SO4+H2O+CO2↑;
(5)判断提取物是否含有碘的方法是:取少量的溶液,向溶液中加入淀粉溶液,若溶液呈蓝色,则有碘存在。

练习册系列答案
相关题目