题目内容
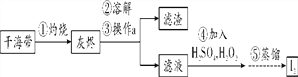
【题目】黑白复印机用的墨粉中常添加Fe3O4粉末。如图是利用氧化沉淀法生产复印用Fe3O4粉末的工业流程图:
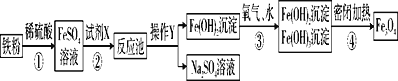
(1)试剂X为________,判断加入试剂X是否过量的方法是_______。
(2)操作Y的名称是________,实验室进行此操作所需的玻璃仪器有玻璃棒、烧杯、________。
(3)第③步的化学反应方程式为 ___________。
(4)在实验室中,铁丝在氧气中燃烧可直接生成四氧化三铁,其实验现象为___________。
【答案】 NaOH(或氢氧化钠) 取反应池中的溶液少量,滴加无色酚酞溶液,若溶液变红,则加入试剂X过量 过滤 漏斗 4Fe(OH)2+O2+2H2O=4Fe(OH)3 剧烈燃烧,火星四射,生成黑色固体,放出热量
【解析】(1)根据已知反应物和生成物分析,根据溶液的酸碱性分析解答;
(2)根据分离固体和液体混合物的方法分析解答;
(3)根据氢氧化亚铁与氧气和水反应生成氢氧化铁解答;
(4)根据铁丝燃烧的实验现象解答。
解:(1)硫酸亚铁溶液与X反应生成氢氧化亚铁沉淀和硫酸钠,故X是氢氧化钠;若氢氧化钠过量,则反应后的溶液显碱性,可取反应池中的溶液少量,滴加无色酚酞溶液,若溶液变红,则加入试剂X过量;
(2)通过操作Y得到固体和液体,故Y是过滤;过滤需要的玻璃仪器有玻璃棒、烧杯、漏斗;
(3) 氢氧化亚铁与氧气和水反应生成氢氧化铁,反应的化学反应方程式为:
4Fe(OH)2+O2+2H2O=4Fe(OH)3;
(4)在实验室中,铁丝在氧气中燃烧可直接生成四氧化三铁,其实验现象为:剧烈燃烧,火星四射,生成黑色固体,放出热量。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目