题目内容
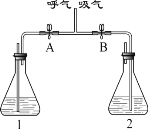
【题目】以下三个实验装置,可用于“测定空气中氧气的含量”。请认真分析,回答下列问题。
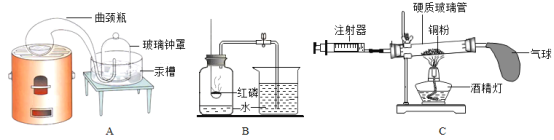
(1)拉瓦锡用装置________(填字母序号)定量研究了空气的成分,在密闭容器中,装置中的汞与空气中的________(填化学式)反应,生成固态物质。人们沿着科学家的足迹,对反应物进行了优化,分别用铜粉、红磷等进行实验,其原理都是采用________(填“物理”或“化学”)的方法,从混合气体中除去某种气体,从而达到物质的分离。
(2)装置B实验:红磷燃烧的现象是________实验结束后,得出的结论是_________________________。
(3)装置C实验,写出该反应的化学方程式_________________,测得数据如下,请完成表格。
硬质玻璃管中空气的体积 | 反应前注射器中空气体积 | 反应后注射器中气体体积 | 实验测得空气中氧气的体积分数 |
25mL | 15mL | 8mL | _____________ |
出现此结果的原因可能是________________________(写出一条即可)。
【答案】A O2 化学 放出大量的热,生成大量白烟 氧气约占空气体积的![]()
![]() 17.5% 未冷却至室温就读数(合理均可)
17.5% 未冷却至室温就读数(合理均可)
【解析】
(1)拉瓦锡是用汞定量研究了空气的成分,所以此处为装置A;汞只能与空气中的氧气发生反应,氧气化学式为O2;因这些测定实验涉及反应均有新物质生成,故这原理都是采用化学方法;
(2)红磷燃烧的现象为:放出大量的热,生成大量白烟;装置B最后发现吸入了大约1/5的水,故得出的结论为氧气约占空气体积的![]() ;
;
(3)铜与空气中氧气反应生成氧化铜,方程式为:![]() ;装置开始时的总体积为25+15=40ml,消耗掉的氧气为15-8=7ml,故消耗氧气的体积分数为7/40×100%=17.5%;空气中氧气的体积分数为21%,则实测值偏小,可能的原因:铜的质量不足、装置未冷却就读数、装置漏气,选一原因填空即可。
;装置开始时的总体积为25+15=40ml,消耗掉的氧气为15-8=7ml,故消耗氧气的体积分数为7/40×100%=17.5%;空气中氧气的体积分数为21%,则实测值偏小,可能的原因:铜的质量不足、装置未冷却就读数、装置漏气,选一原因填空即可。

 阅读快车系列答案
阅读快车系列答案