题目内容
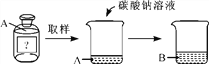
【题目】实验室中同学们进行了如图所示实验,用正确的试剂成功探究出了在空气中久置的氢氧化钠固体的变质情况。下列说法正确的是( )

A.甲溶液可以选择Ca(OH)2溶液或CaCl2溶液
B.若II、III均有明显现象,则说明样品部分变质
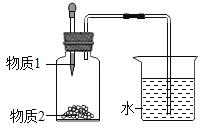
C.D物质可能是气体,也可能是沉淀
D.溶液B中的溶质至少有两种
【答案】BD
【解析】
氢氧化钠吸收空气中的二氧化碳而变质成为碳酸钠,所以变质程度有两种情况:一、部分变质,氢氧化钠和碳酸钠都有;二、全部变质,只有碳酸钠。
A. 甲溶液可以选择CaCl2溶液(中性),氯化钙将碳酸钠全部转化为碳酸钙沉淀,且不会对氢氧化钠的检验造成干扰;不能选择Ca(OH)2溶液,原因是碳酸钠与氢氧化钙反应会生成碳酸钙和氢氧化钠,会对检验原溶液中是否含氢氧化钠造成干扰。故A不符合题意;
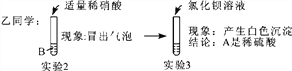
B. 反应II有白色沉淀产生,原因是变质后的碳酸钠与氯化钙反应生成碳酸钙白色沉淀和氯化钠,证明样品中含有碳酸钠;实验III酚酞溶液会变红,说明溶液中含有未变质的氢氧化钠。氢氧化钠和碳酸钠都有则说明样品部分变质。故B符合题意;
C. 若D物质是气体,则甲溶液是过量的稀盐酸,碳酸钠与稀盐酸反应生成二氧化碳气体,证明样片含有碳酸钠;因为盐酸过量,盐酸与氢氧化钠反应生成氯化钠和水,无法检验原样品中是否含有氢氧化钠。故C不符合题意;
D. 溶液B中一定含有碳酸钠与氯化钙反应的生成物氯化钠,还含有未反应的甲溶液氯化钙,即溶质至少有两种。故D符合题意。
故选BD。

 初中学业考试导与练系列答案
初中学业考试导与练系列答案【题目】以下三个实验装置,可用于“测定空气中氧气的含量”。请认真分析,回答下列问题。
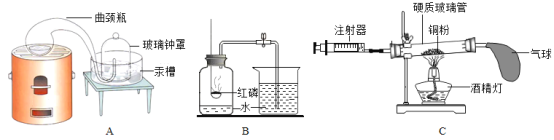
(1)拉瓦锡用装置________(填字母序号)定量研究了空气的成分,在密闭容器中,装置中的汞与空气中的________(填化学式)反应,生成固态物质。人们沿着科学家的足迹,对反应物进行了优化,分别用铜粉、红磷等进行实验,其原理都是采用________(填“物理”或“化学”)的方法,从混合气体中除去某种气体,从而达到物质的分离。
(2)装置B实验:红磷燃烧的现象是________实验结束后,得出的结论是_________________________。
(3)装置C实验,写出该反应的化学方程式_________________,测得数据如下,请完成表格。
硬质玻璃管中空气的体积 | 反应前注射器中空气体积 | 反应后注射器中气体体积 | 实验测得空气中氧气的体积分数 |
25mL | 15mL | 8mL | _____________ |
出现此结果的原因可能是________________________(写出一条即可)。