题目内容
【题目】食醋是厨房中常用的调味品,它的主要成分是乙酸,乙酸分子的模型如图所示,其中![]() 代表一个碳原子,
代表一个碳原子,![]() 代表一个氢原子,
代表一个氢原子,![]() 代表一个氧原子, 下列说法不正确的是( )
代表一个氧原子, 下列说法不正确的是( )

A.乙酸是一种化合物
B.乙酸由2个碳原子、4个氢原子、2个氧原子构成
C.乙酸中的碳、氢、氧元素的质量比为1:2:1
D.乙酸中碳元素的质量分数为40%
【答案】BC
【解析】
A、从图中看出乙酸由碳元素、氧元素和氢元素组成,符合化合物“由两种或两种以上的元素组成的纯净物”的定义,A选项正确,不合题意;
B、“乙酸”是宏观的表述,“原子”是微观的表述,宏观和微观不能混用,B选项错误,符合题意;
C、由图可知每个乙酸分子由2个碳原子、4个氢原子、2个氧原子构成的,则碳、氢、氧元素的个数比为1:2:1,质量比应为12:2:16=6:1:8,C选项错误,符合题意;
D、乙酸中碳元素的质量分数=![]() ,D选项正确,不合题意;
,D选项正确,不合题意;
故选B、C。

【题目】某钙片的标签如图所示,此钙片成分中只有碳酸钙含有钙元素.

(1)请通过计算说明此标签中的含钙量是否错误_____.
(2)为测定其真实的含钙量,小东每次取10片钙片放入已称量的含足量稀盐酸的烧杯中,充分反应后再称取烧杯和剩余物的总质量![]() 小东做了三次实验,数据如下:
小东做了三次实验,数据如下:
物质的质量 | 第一次 | 第二次 | 第三次 | 平均值 |
反应前:烧杯+盐酸 | 22g | 22g | 22g | 22g |
10片钙片 | 8g | 8g | 8g | 8g |
反应后:烧杯十剩余物 | 26.7g | 26.5g | 26.9g | 26.7g |
①列式计算每片此钙片含碳酸钙的质量_____.
②请列式计算每片此钙片的含钙量,并建议厂家如何改标签_____.
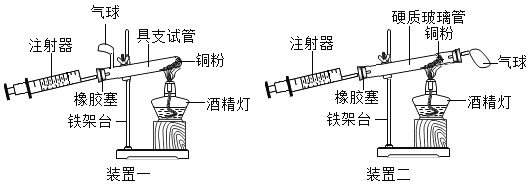
【题目】小雨阅读课外资料得知:氯酸钾的分解可用二氧化锰、氧化铜等物质作催化剂。于是,他对影响氯酸钾分解的因素及催化剂的催化效果产生了探究兴趣。
(提出问题)氧化铜是否比二氧化锰催化效果更好?影响氯酸钾分解速率的因素有哪些呢?
(设计实验)小雨以生成等体积的氧气为标准,设计了下列几组实验。
序号 | KClO3的质量 | 其他物质的质量 | 温度 | 氧气的体积 | 反应所需时间 |
① | 10.0g | 330℃ | 100mL | t1 | |
② | 10.0g | CuO1.5g | 330℃ | 100mL | t2 |
③ | 10.0g | MnO21.5g | 330℃ | 100mL | t3 |
④ | 10.0g | MnO2_____g | 380℃ | 100mL | t4 |
(1)若t1>t2,说明氧化铜能加快氯酸钾的分解速率。若要确定氧化铜是此反应的催化剂,还需探究反应前后,氧化铜的_____和_____不变。
(2)写出实验④所涉及的化学反应的文字表达式_____。
(3)实验④中MnO2的质量为_____g,若t3>t4,则化学反应快慢与温度的关系是_____。
(4)氯酸钾的分解速率可能还与_____因素有关,请设计实验证明_____。
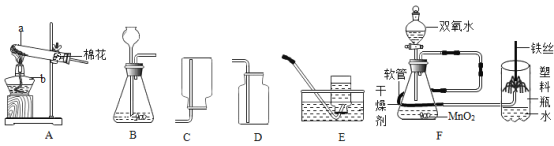
【题目】以下三个实验装置,可用于“测定空气中氧气的含量”。请认真分析,回答下列问题。
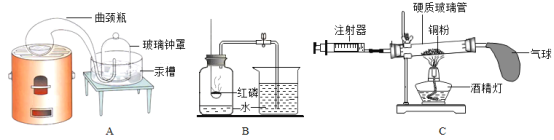
(1)拉瓦锡用装置________(填字母序号)定量研究了空气的成分,在密闭容器中,装置中的汞与空气中的________(填化学式)反应,生成固态物质。人们沿着科学家的足迹,对反应物进行了优化,分别用铜粉、红磷等进行实验,其原理都是采用________(填“物理”或“化学”)的方法,从混合气体中除去某种气体,从而达到物质的分离。
(2)装置B实验:红磷燃烧的现象是________实验结束后,得出的结论是_________________________。
(3)装置C实验,写出该反应的化学方程式_________________,测得数据如下,请完成表格。
硬质玻璃管中空气的体积 | 反应前注射器中空气体积 | 反应后注射器中气体体积 | 实验测得空气中氧气的体积分数 |
25mL | 15mL | 8mL | _____________ |
出现此结果的原因可能是________________________(写出一条即可)。