题目内容
【题目】图是某化工厂生产烧碱的工业流程图.
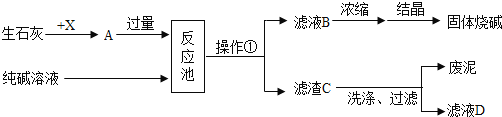
请根据以上信息回答下列问题:
(1)请写出X物质在实验室中的一种用途 .
(2)反应池中发生反应的化学方程式为 .
(3)操作①的名称是 ,结晶得到的固体烧碱中可能含有少量的 (写化学式).
(4)滤液D可加入反应池循环再利用,目的是降低生产成本和防止 .
【答案】(1)洗涤仪器(或做溶剂) (2)Ca(OH)2+Na2CO3=CaCO3↓+2NaOH
(3)Ca(OH)2 (4)环境污染
【解析】
试题分析:(1)工业上生成氢氧化钠的反应原理是氢氧化钙和碳酸钠反应生成氢氧化钠和碳酸钙沉淀,氧化钙与水反应能生成氢氧化钙,故X是水,水在实验室中常用于清洗仪器以及配制溶液等,故填:洗涤仪器(或做溶剂);
(2)反应池中氢氧化钙和碳酸钠反应生成碳酸钙沉淀和氢氧化钠,故填:Ca(OH)2+Na2CO3=CaCO3↓+2NaOH;
(3)经过操作①,得到了滤液B和滤渣C,则操作①是过滤,由于氢氧化钙是微溶于水的物质,得到的滤液中含有少量的氢氧化钙,直接蒸发结晶,则得到的固体烧碱中含有氢氧化钙,故填:过滤,Ca(OH)2;
(4)对滤液D进行循环利用,可以减少对环境的污染,故填:环境污染.

练习册系列答案
相关题目