题目内容
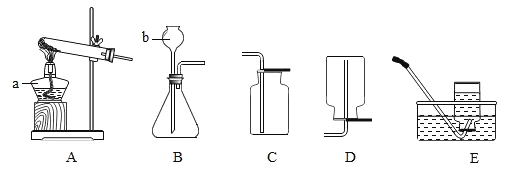
【题目】将一种无色无味的液体A装入试管,用带火星的木条伸入试管,无现象,而向其中加入少量黑色粉末B后,迅速产生气泡,生成了使带火星的木条复燃的气体C,使金属E红热并伸入盛有气体C且瓶底有少量液体D的集气瓶中,金属E剧烈燃烧,火星四射,生成黑色固体F。
(1)写出它们的化学式: A._________________,B.________________,C.__________________,D.________________,F._________________。
(2)写出文字中涉及反应的化学方程式
①__________________________________________________________。
②__________________________________________________________。
【答案】 H2O2 MnO2 O2 H2O Fe3O4 2H2O2 ![]() 2H2O+O2↑ 3Fe+2O2
2H2O+O2↑ 3Fe+2O2 ![]() Fe3O4
Fe3O4
【解析】无色无味的液体A用带火星的木条试验,无明显现象,而向其中加入少量黑色粉末B后,迅速产生气泡,生成了使带火星的木条复燃的气体C,因此C是氧气,则B是二氧化锰,A是过氧化氢;金属E能够在氧气中剧烈燃烧,火星四射,生成黑色固体F,因此E是铁,F是四氧化三铁,铁铁丝在氧气中燃烧,集气瓶底常放在少量的水,防止集气瓶底炸裂,所以D是水,因此:(1)化合物的化学式书写:显正价的元素其符号写在左边,显负价的写在右边,化合价的绝对值交叉约减,得化学式右下角的数字,数字为1时不写。所以化学式分别为: A. H2O2,B. MnO2,C. O2,D. H2O,F. Fe3O4;(2)①过氧化氢在二氧化锰作用下分解的反应的化学方程式为:2H2O2 ![]() 2H2O+O2↑;②铁在氧气中燃烧产生四氧化三铁,反应的方程式为:3Fe+2O2
2H2O+O2↑;②铁在氧气中燃烧产生四氧化三铁,反应的方程式为:3Fe+2O2![]() Fe3O4;
Fe3O4;